图甲表示的是H2O2分解反应过程中的能量变化。在不同温度下,分别向H2O2溶液(20g·L-1)中加入相同体积且物质的量浓度均为0.5mol·L-1的不同溶液,反应中H2O2浓度随时间的变化如图乙所示。
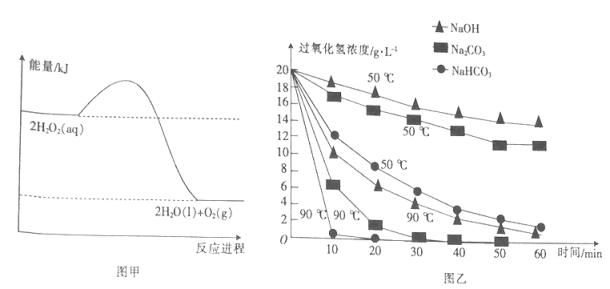
从图中得出的结论不正确的是
A.H2O2的分解反应为放热反应
B.断裂共价键所需的能量:2×E(O—O)<1×E(O=O)
C.加入相同物质时,温度越高,H2O2分解的速率越快
D.相同温度下,加入不同物质的溶液,碱性越强,H2O2分解的速率越快
高三化学选择题简单题
图甲表示的是H2O2分解反应过程中的能量变化。在不同温度下,分别向H2O2溶液(20g·L-1)中加入相同体积且物质的量浓度均为0.5mol·L-1的不同溶液,反应中H2O2浓度随时间的变化如图乙所示。

从图中得出的结论不正确的是
A.H2O2的分解反应为放热反应
B.断裂共价键所需的能量:2×E(O—O)<1×E(O=O)
C.加入相同物质时,温度越高,H2O2分解的速率越快
D.相同温度下,加入不同物质的溶液,碱性越强,H2O2分解的速率越快
高三化学选择题简单题
图甲表示的是H2O2分解反应过程中的能量变化。在不同温度下,分别向H2O2溶液(20g·L-1)中加入相同体积且物质的量浓度均为0.5mol·L-1的不同溶液,反应中H2O2浓度随时间的变化如图乙所示。

从图中得出的结论不正确的是
A.H2O2的分解反应为放热反应
B.断裂共价键所需的能量:2×E(O—O)<1×E(O=O)
C.加入相同物质时,温度越高,H2O2分解的速率越快
D.相同温度下,加入不同物质的溶液,碱性越强,H2O2分解的速率越快
高三化学选择题简单题查看答案及解析
下述实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 | 研究催化剂对H2O2分解速率的影响 |
| B | 将溴水加入KIO3溶液中 | 比较碘与溴单质氧化性的强弱 |
| C | 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 | 研究温度对化学平衡的影响 |
| D | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有氧化性 |
高三化学选择题中等难度题查看答案及解析
根据下列图示所得出的结论正确的是
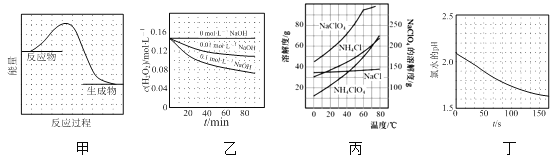
A.图甲表示某反应过程中的能量变化曲线,可推知该反应是吸热反应
B.图乙表示70℃时不同碱性条件下H2O2的浓度随时间变化的曲线,可推知溶液碱性越强,H2O2分解速率越慢
C.图丙表示部分物质的溶解度随温度变化的曲线,可推知20℃时向含a mol NaClO4的饱和溶液中加入a mol NH4Cl固体会有NH4ClO4固体析出
D.图丁表示光照下氯水的pH随时间的变化曲线,可推知光照后溶液中Cl2浓度增大
高三化学单选题中等难度题查看答案及解析
向20 mL 0.40 mol/L H2O2溶液中加入少量KI溶液:ⅰ.H2O2+I-=H2O+IO﹣;ⅱ.H2O2+IO﹣= H2O+O2↑+ I﹣。H2O2分解反应过程中能量变化和不同时刻测得生成O2的体积(已折算标准状况)如下。
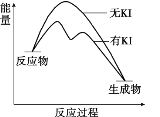
| t/min | 0 | 5 | 10 | 15 | 20 |
| V(O2)/mL | 0.0 | 12.6 | 20.16 | 28.0 | 32.7 |
下列判断不正确的是
A. 从图中可以看出,KI能增大H2O2的分解速率
B. 反应ⅰ是放热反应,反应ⅱ是吸热反应
C. 0~10 min的平均反应速率:v(H2O2)≈9.0×10-3 mol/(L·min)
D. H2O2在反应过程中既体现了氧化性,又体现了还原性
高三化学单选题中等难度题查看答案及解析
向20mL 0.40mol/L H2O2溶液中加入少量KI溶液:
i.H2O2+I-=H2O+IO-
ii.H2O2+ IO-=H2O+O2↑+ I-
H2O2分解反应过程中能量变化和不同时刻测得生成O2的体积(已折算标准状况)如下
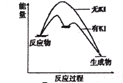

下列判断不正确的是
A.从图中可以看出,KI能增大H2O2的分解速率
B.反应i是放热反应,反应ⅱ是吸热反应
C.0-10min的平均反应速率:v(H2O2)≈9.0×10-3 mol· L-1·min-1
D.H2O2在反应过程中既体现了氧化性,又体现了还原性
高三化学单选题中等难度题查看答案及解析
已知常温下HF酸性强于HCN,分别向1Ll mol/L的HF和HCN溶液中加NaOH固体调节pH(忽略温度和溶液体积变化),溶液中(X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是

A.直线I对应的是
B.I中a点到b点的过程中水的电离程度逐渐增大
C.c点溶液中:
D.b点溶液和d点溶液相比:cb(Na+)<cd(Na+)
高三化学单选题困难题查看答案及解析
已知常温下,酸性:HF>HCN,分别向1L1mol/L的HF和HCN溶液中加NaOH固体调节pH(忽略温度和溶液体积的变化),溶液中的(X表示F或CN)随pH变化如图所示,下列说法正确的是

A.HF的电离常数Ka(HF)的数量级10-4
B.d点溶液中:c(Na+)=c(X-)>c(HX)
C.a到b点的过程中水的电离程度先变大后变小
D.b点溶液和d点溶液中c(Na+):b<d
高三化学单选题中等难度题查看答案及解析
已知常温下HF酸性强于HCN,分别向1Ll mol/L的HF和HCN溶液中加NaOH固体调节pH(忽略温度和溶液体积变化),溶液中(X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是
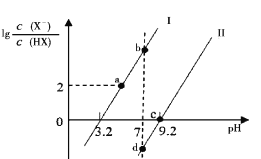
A.直线I对应的是
B.I中a点到b点的过程中水的电离程度逐渐增大
C.c点溶液中:
D.b点溶液和d点溶液相比:cb(Na+)<cd(Na+)
高三化学单选题困难题查看答案及解析
(1)工业合成氨时,合成塔中每产生1molNH3,放出46.1kJ的热量。
某小组研究在500℃下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
| 容器 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系能量的变化/kJ | ||
| N2 | H2 | NH3 | |||
| a | 1 | 4 | 0 | t1 min | 放出热量:36.88kJ |
| b | 2 | 8 | 0 | t2 min | 放出热量:Q |
①容器a中,0~t1时间的平均反应速率为υ(H2)= ___________。
②下列叙述正确的是________(填字母序号)。
A.容器b中反应达平衡状态时,Q>73.76kJ
B.平衡时,两容器中H2的体积分数相等
C.反应开始时,两容器中反应的化学反应速率相等
D.平衡时,容器中N2的转化率:a<b
(2)以氨为原料,合成尿素的反应原理为:2NH3(g)+CO2(g)CO(NH2)2(l)+H2O(g) ΔH = a kJ·mol-1。
为研究平衡时CO2的转化率与反应物投料比[]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应。(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
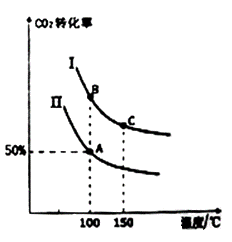
①a_______0 (填“>”或“<”)。
②若n(CO2)起始 =10 mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为_______。
③A点平衡常数与B点平衡常数间的关系:KA_______ KB (填“>”或“<”或“=”)。
(3)利用氨气与空气催化氧化法制取联氨N2H4.如图是由“联氨—空气”形成的绿色燃料电池,以石墨为电极的电池工作原理示意图,b电极为_______极(填“正”或“负”),写出该电池工作时a电极的电极反应式_______。
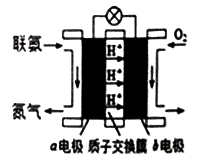
高三化学简答题困难题查看答案及解析
分别向等体积1mol/L盐酸和1mol/L醋酸溶液中加入等量的镁条,反应时间与溶液pH变化关系如右图。下列说法中不正确的是
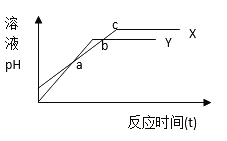
A. Y代表盐酸与镁条的反应 B. a点时反应Y消耗镁条的量少
C. b点表示此时两溶液pH相等 D. c点表示此时反应结束
高三化学单选题中等难度题查看答案及解析