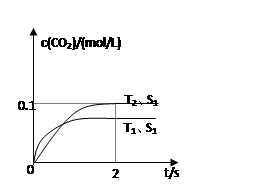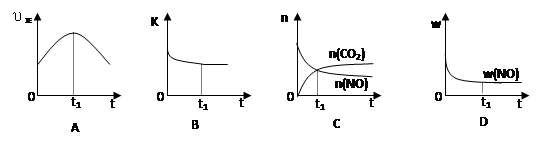-
X、Y、Z、W、Q五种前四周期元素,原子序数依次增大。已知五种元素中只有一种为金属元素,XW2分子与Y3为等电子体,元素W的原子序数等于元素Z的原子序数加8,Q的最外层电子数为2,次外层电子数等于Y和W2-最外层电子数之和。根据以上信息回答下列问题:
(1)X、Y、Z的电负性由大到小的顺序为 。
(2)XW2的电子式为 ,Y3的分子构型为 型。
(3)Q的价电子排布式为 。
(4)下列关于WZ2结构的说法正确的是
A.WZ2为直线型非极性分子 B.WZ2为直线型极性分子
C.WZ2中W为sp3杂化 D.WZ2中W为sp2杂化
(5)α-QW的晶胞是立方体,用X射线粉末法测得该晶体晶胞边长a=520.0pm,26℃测得该晶体的密度为4.1g/cm3,请列式计算一个晶胞中含有的Q、W离子数。
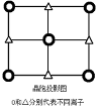
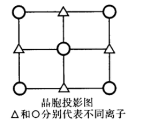
(6)α-QW晶胞的一个侧面的投影图如右图所示,与Q离子距离最近且距离相等的W离子构成的几何图形是 。
-
【化学选修3-物质结构与性质】(15分)X、Y、Z、W、Q五种前四周期元素,原子序数依次增大.已知X、Y、Z、W均为非金属元素,XW2分子与Y3为等电子体,元素W的原子序数等于元素Z的原子序数加8,Q的最外层电子数为2,次外层电子数等于Y和W2 -最外层电子数之和,根据以上信息回答下列问题:
(1)上述五种元素中电负性最大的是____(填元素符号,下同),Y的第一电离能大于Z的第一电离能原因 。
(2)XW2的电子式为 。Y3的分子构型为 。
(3)Q的价电子排布式为 。
(4)下列关于WZ2结构的说法正确的是 。
a.WZ2直线形非极性分子
c.WZ2中w为sp3杂化
b.WZ2直线形极性分子
d.WZ2中W为sp2杂化
(5)d-QW的晶胞是立方体,用X射线衍射法测得该晶体晶胞边长a=520.0pm,26℃测得该晶体的密度为4.1g/cm3,请列式计算一个晶胞中含有的Q、W离子数。(5.23=140.6)
(6)d-QW的晶胞的一个侧面的投影图如图所示,与Q离子距离最近且距离相等的W离子构成的几何图形是________________
-
现有A、B、C、D、E五种短周期元素,已知他们的原子序数依次增大,元素A的原子只有一个电子层;又知元素A能分别与元素B、C、D形成电子总数相等的化合物分子X、Y、Z,Y有刺激性气味,Z常温下为液态,元素E的单质的水溶液有漂白性.
请回答下列问题:
(1)元素E的单质的饱和溶液与石灰石反应后所得溶液的漂白性增强的原因是______;
(2)在锅炉水中加入C2A4,可以把锅炉表面的氧化铁还原为结构紧密的四氧化三铁保护层,C2A4 被氧化,且反应中无污染物生成,写出反应的化学方程式(不必配平)______,1mol C2A4 参加反应转移电子的数目为______,氧化产物的化学式为______;
(3)化合物Y与元素C的最高正价氧化物的水化物按物质的量比为2:1完全反应后的水溶液呈______ 性(填“酸”“碱”或“中”),溶液中离子浓度由大到小的顺序为______;
(4)用X、D2和能传导O2-的固体电解质组成的原电池中,负极的电极反应式为______.
(5)A、B、D三种元素可以形成最简式为B2A4D且有香味的有机物,该有机物在酸性条件下可以水解,生成含碳原子数相同的两种常见有机物,这两种有机物均可用作食品调味剂.则这种有香味的有机物在一定条件下水解的化学方程式是______
-
X、Y、Z、W是元素周期表前四周期常见的四种元素,原子序数依次增大。X原子核外有两种形状的电子云,四种伸展方向,常温下以双原子分子存在,性质稳定;Y的单质是生活中常见的合金材料成分之一,原子核外只有一个未成对电子,Z原子的半径比X大,其基态原子最外层的p电子是该层s电子的两倍,W是最常见的黑色金属之一。
(1)Z位于元素周期表中的位置是________,W3+的最外层电子排布式是______,X的氧化物XO2与H2O比较,熔点较高的是______ (填化学式)。
(2)加热条件下,Z的单质与足量的X的最高价氧化物的水化物的浓溶液反应,生成 Z的最髙价含氧酸,写出此反应的化学方程式________。.
(3)比较Y、W性质的活泼性________(用一个化学反应方程式表示)。
(4)2013年初,全国各地多个城市都遭遇“十面霾伏”,造成“阴霾天”的主要根源之一是汽车尾气和燃煤尾气排放出来的固体小颗粒PM2.5。汽车尾气净化的主要原理为:2NO(g)+2CO(g)  2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
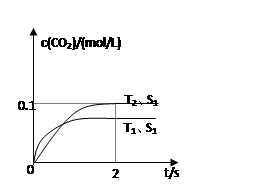
据此判断:
该反应为________反应(放热、吸热);在T2温度下,0~2s内的平均反应速率:υ(N2)=________;
(5)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,
在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
(6)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填代号)。
(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量和质量)
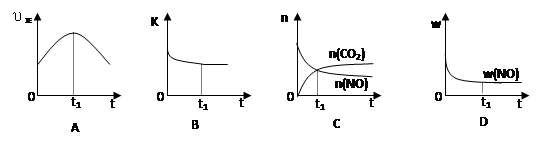
-
已知A、B、C、D、E是原子序数依次增大的五种元素,A元素核内只有质子;B元素的某种核素可用于考古;D原子核外电子排布为nsnnpn+2。E是第四周期元素,最外层只有一个电子,其余各层电子均充满。请回答下列问题(用元素符号或化学式表示):
(1)元素B、C、D的基态原子的电负性由大到小的顺序为 (用元素符号表示)。
化合物CA3的沸点比化合物BA4的高,其主要原因是 。
(2)A、B、D三种元素组成的一种化合物是新装修居室中常含有的一种有害气体。则分子中B原子轨道的杂化类型为 。
(3)E的核外电子排布式为 。E2D为半导体材料,在其立方晶胞内部有4个D原子,其余D原子位于面心和顶点,则该晶胞中有______个E原子。E2D能与稀硫酸反应得E,E的晶胞为面心立方最密堆积,已知该晶体的密度为9.00g/cm3,则E原子的半径为 cm。
(4)C2A4与ED在碱性溶液中反应生成无色气体和红色沉淀,则该反应的化学方程式可表示为: 。
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,其中只有一种金属元素,X是周期表中原子半径最小的元素,Y的最高正价与最低负价绝对值相等,W最外层电子数是最内层电子数的3倍,R是同周期元素中原子半径最小的元素。下列说法不正确的是
A. 原子半径Z>W>R
B. 对应的氢化物的热稳定性:R>W>Y
C. 单质Z可与R的最高价含氧酸发生置换反应
D. W与R所形成的简单离子均能影响水的电离平衡
-
已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期p区的元素且最外层只有2对成对电子,F是29号元素。
(1)B、C、D三元素第一电离能由大到小的顺序为 (用元素符号表示)
(2)BD32-中心原子杂化轨道的类型为________杂化;CA4+的空间构型为______________。
(3)基态E原子的价电子排布图______________________________。
(4)1mol BC-中含有π键的数目为______________。
(5)比较D、E元素最简单氢化物的沸点高低: (用化学式表示)。
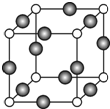
(6)C、F两元素形成的某化合物的晶胞结构如图所示,顶点为C原子。则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为________________g/cm3(用含a、NA的符号表示)。
-
已知W、X、Y、Z为原子序数依次增大的四种短周期元素。W、Z同主族,X、Y、Z同周期,其中只有X为金属元素,Z元素原子的最外层电子数是其电子层数的2倍。下列说法不正确的是
A.X与W形成化合物与稀盐酸反应不可能产生氧气
B.原子半径:X>Y>Z>W
C.简单氢化物的稳定性:W>Z>Y
D.Y与W形成化合物能与NaOH溶液反应
-
已知X、Y、Z、W是短周期中四种非金属元素,它们的原子序数依次增大,X元素原子价电子排布式为ns1,Y元素是空气中含量最多的元素,Z 与W同主族,而且W原子的电子排布式中,p轨道上只有1个未成对电子.
(1)由元素X和元素Y形成的常见化合物电子式是______,它极易液化,也极易溶于水,是因为它的分子间,或它与水分子间容易形成______键,它与XW化合生成的化合物属于______晶体;
(2)Z元素的基态原子的电子排布式是______,据有关资料记载,它与硫原子能形成AB6型分子的八面体结构,S原子位于八面体的中心,其立体结构如图:
则该分子是______(填极性或者非极性)分子,S表现的化合价是______.
若该分子中的两个B被两个C取代,形成AB4C2型分子,则AB4C2型分子有______种同分异构体.

-
X、Y、Z、W是原子序数依次增大的四种不同主族短周期元素,已知四种元素原子的最外层电子数之和为12,X原子的半径最大,只有W是非金属元素。请回答:
(1)Y元素在周期表中的位置是_________________
(2)四种元素的简单离子中,半径最小的是______离子(填具体的离子符号)
(3)用化学方程式表示工业上获得X单质的方法是________________
(4)Z、W的最高价氧化物对应的水化物恰好反应得到溶液显______性,用离子方程式解释其原因_________
(5)0.1mol/L的X、W组成的化合物溶液中,离子浓度由大到小的顺序为__________
(6)甲是X元素最高价氧化物对应的水化物,将常温下pH=a的甲溶液加热至90℃,其pH值将______(填“增大”“减小”或“不变”)。
常温下,向1Lamol/L的醋酸溶液中加入bg甲固体,反应后溶液呈中性,则醋酸的电离常数Ka=_________(用含a、b字母的代数式表示,体积变化忽略不计)