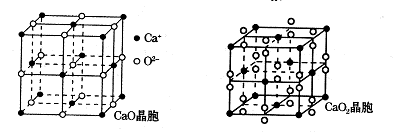-
CaC2可用于固氮:CaC2+N2  CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。
CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:________________。
(2)C、N、O三种元素的第一电离能由小到大的顺序是________。
(3)NH3中N原子的杂化方式为________________;根据价层电子对互斥理论推测CO32-的空间构型为________。
(4)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有________________(填写一种化学式即可);写出CaCN2水解反应的化学方程式________________。
-
CaC2可用于固氮:CaC2+N2 CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。
CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式: 。
(2)C、N、O三种元素的第一电离能由小到大的顺序是 。
(3)NH3中N原子的杂化方式为 ;根据价层电子对互斥理论推测CO32-的空间构型为 。
(4)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有 (填写一种化学式即可);写出CaCN2水解反应的化学方程式
-
(14分)曾经有一种固氮的方法:1100°C通N2和CaC2反应得到CaCN2 。
已知:CaCN2+3H2O = 2NH3+CaCO3 ;CaC2+2H2O = C2H2↑+Ca(OH)2
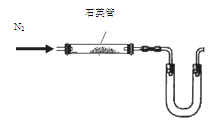
(1)某同学采用以下装置(加热和夹持仪器已略去)制取少量的CaCN2
①U形管中盛放的物质是 (填一种);
② (填“能”或“不能”)用普通玻璃管代替图中石英管;
(2)检验反应后的固体(用W表示)中含有氮元素该同学将适量W溶于水,有气泡产生,说明固体中含有氮元素,该结论不正确。若要得出正确结论,还需进行的实验是 。
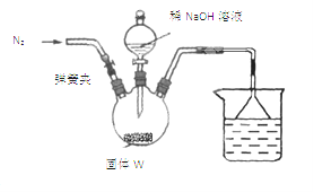
(3)测定W中CaCN2的质量分数
步骤Ⅰ:按如图所示装置(夹持仪器已略去)进行实验:关闭弹簧夹,将漏斗中溶液逐滴加入到三颈瓶中,当W反应完全后,打开弹簧夹,通入氮气,直至氨气被200mL0.1 mol·L-1硫酸完全吸收。
步骤Ⅱ:准确量取烧杯中溶液20.00mL置于锥形瓶中,滴入几滴指示剂,用cmol·L-1NaOH溶液滴定过量的硫酸,实验测得消耗标准溶液的平均体积为vmL。
已知三种常用指示剂变色pH范围如下:
| 指示剂 | a | b | c |
| 变色pH范围 | 3.1~4.4 | 8.0~10.0 | 4.4~6.2 |
| 说明 | pH<3.1显红色 pH>4.4显黄色 | pH<8.0显无色 pH>10.0显红色 | pH<4.4显红色 pH>6.2显黄色 |
①上述滴定过程中,不宜选用的指示剂是 (填字母序号);
②烧杯中最终吸收氨气的物质的量为 mol;经进一步计算可求得W中CaCN2质量分数。
③上述实验所得结果明显偏小,若不考虑装置的气密性和操作误差,则导致结果偏小的可能原因是
(写1种)。
-
下列说法错误的是
A. 反应CaC2(s) + N2(g) = CaCN2(s) + C(s) 的 H<0
H<0
B. 海上石油钢铁钻井平台可用外加电流的阴极保护法以防腐
C. H2O2催化分解每产生1molO2,转移电子的数目为2×6.02×1023
D. 25℃时,加水稀释0.1mol·L-1NH4Cl,溶液中 不断增大
不断增大
-
氨有着广泛的用途,可用于化肥、硝酸、合成纤维等工业生产。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应可生成氨气:

该反应在固定体积的密闭容器中进行,有关说法正确的是_____________(填序号字母)。
A.反应处于平衡状态时,
B.反应达到平衡后,
C.体系的总压强不变,说明反应已达平衡
D.混合气体的密度保持不变,说明反应已达平衡
(2)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧试验机中相关的反应有:
 ①
①
 ②
②
 ③
③
请写出上述三个反应中 、
、 、
、 三者之间关系的表达式,
三者之间关系的表达式, =_________。
=_________。
(3)工业制硝酸的主要反应是:
 =
=
①升高温度,反应的K值减小,则Q______(填“>”、“<”或“=”)0。
②若反应起始的物质的量相同,下列关系图错误的是________(填序号)。


③在容积固定的密闭容器中发生上述反应,容器内部分物质的浓度如下表:
| 时间/浓度 | 

| 

| 

| 

|
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | a | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
反应在第2 min到第4 min时,O2的平均反应速率为________。
反应在第2 min时改变了条件,改变的条件可能是______________________________。
该条件下,反应的平衡常数K=________。
-
下列有关说法正确的是
A.反应CaC2(s)+N2(g)=CaCN2(s)+C(s)能自发进行,则该反应ΔS>0
B.常温下向0.1 mol·L-1CH3COOH溶液中通入少量HCl气体,c(H+)·c(CH3COO-)增大
C.将1 mol Cl2溶于水中,反应中转移的电子数为6.02×1023个
D.2H2(g)+O2(g)=2H2O(g)的反应物键能总和大于生成物键能总和
-
下列有关说法正确的是 ( )
A.反应CaC2(s)+N2(g)===CaCN2(s)+C(s)能自发进行,是因为ΔH<0
B.若电工操作中将铝线与铜线直接相连,会导致铜线更快被氧化
C.向水中加入NaHCO3或NaHSO4固体后,水的电离程度均增大
D.对于乙酸乙酯的水解反应,加入稀硫酸会使平衡向正反应方向移动
-
下列有关说法正确的是
A.反应CaC2(s)+N2(g)=CaCN2(s)+C(s)能自发进行,是因为△H<0
B.若电工操作中将铝线与铜线直接相连,会导致铜线更快被氧化
C.向水中加入NaHCO3或NaHSO4固体后,水的电离程度均增大
D.对于乙酸乙酯的水解反应,加入稀硫酸会使平衡向正反应方向移动
-
[化学——选修3物质结构与性质l(15分)三聚氰胺(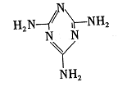 )俗称。蛋白精”,可以由下列反应合成:CaO+3C
)俗称。蛋白精”,可以由下列反应合成:CaO+3C CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式: ;CaCN2中阴离子为CN22一,与CN22一互为等电子体的分子有N2O和 (填化学式),由此可以推知CN22一的空间构型为____。
(2)三聚氰胺中氮原子的杂化方式有 。
(3)一些不法商家常在牛奶中加入三聚氰胺和三聚氰酸来提高“蛋白质”的含量,人在摄人三聚氰胺和三聚氰酸( )后,两者之间易通过 结合,在肾脏内易形成结石。
)后,两者之间易通过 结合,在肾脏内易形成结石。
(4)钙的氧化物有CaO和CaO2两种,其晶胞结构如下图所示,CaO晶体中Ca2+的配位数为 ,Ca2+采取的堆积方式为 。已知CaO2密度是ρg·cm-3,晶胞结构如图所示,则CaO2晶胞中距离最近的两个钙离子间的距离为 cm(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
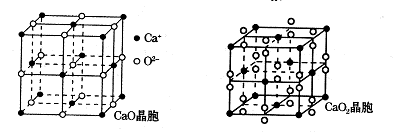
(5)配位化合物K3[ Fe( CN)n]遇亚铁离子会产生蓝色沉淀,因此可用于检验亚铁离子,已知铁原子的最外层电子数和配体提供电子数之和为14,求n= 。
-
(15分)可以由下列反应合成三聚氰胺:CaO+3CCaC2+CO↑,CaC2+N2CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:______________________________________________________________________。
CaCN2中阴离子为CN,与CN互为等电子体的分子有N2O和________(填化学式),由此可以推知CN的空间构型为________。
(2)尿素分子中C原子采取________杂化。尿素分子的结构简式是________________。
(3)三聚氰胺  俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 后,
后,
三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为______________。
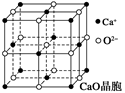
已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离 __________________________(列出计算式)
CaO晶体和NaCl晶体的晶格能分别为:CaO 3 401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是____________________________。
CaCN2+C,CaCN2(氰氨化钙)和水反应可生成NH3。




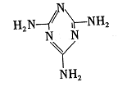 )俗称。蛋白精”,可以由下列反应合成:CaO+3C
)俗称。蛋白精”,可以由下列反应合成:CaO+3C )后,两者之间易通过
)后,两者之间易通过