-
在3 L容积不变的容器中,发生 N2 + 3H2 == 2NH3的反应。现通入10mol H2 和 10 mol N2 , 用H2 表示的反应速率为0.3mol/(L·s) ,则10 s末容器中N2的物质的量是
A.7mol B.5mol C.4mol D.1mol
高三化学选择题简单题查看答案及解析
-
一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应3H2(g)+N2(g)⇌2NH3(g) ΔH=-92.4 kJ·mol-1,测得反应的相关数据如下:
容器1
容器2
容器3
反应温度T/K
500
500
300
反应物投入量
3 mol H2、1 mol N2
4 mol NH3
2 mol NH3
平衡v正(N2)/mol·L-1·s-1
v1
v2
v3
平衡c(NH3)/mol·L-1
c1
c2
c3
平衡体系总压强p/Pa
p1
p2
p3
达到平衡时能量变化
放出a kJ
吸收b kJ
吸收c kJ
达到平衡时体积分数
φ1(NH3)
φ2(NH3)
φ3(NH3)
物质的平衡转化率α
α1(H2)
α2(NH3)
α3(NH3)
平衡常数K
K1
K2
K3
下列说法正确的是( )
A. v1<v2,c2>2c1 B. K1=K2,p2>2p1
C. φ1(NH3)<φ3(NH3),a+0.5b<92.4 D. c2>2c3,α1(H2)+α3(NH3)>1
高三化学多选题困难题查看答案及解析
-
在温度、容积相同的三个密闭容器中发生反应N2(g) + 3H2(g)
2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器
甲
乙
丙
反应物投入量
1molN2、3molH2
2molNH3
4molNH3
NH3的浓度(mol/L)
c1
c2
c3
反应的能量变化
放出a kJ
吸收b kJ
吸收c kJ
体系压强
P1
P2
P3
反应物转化率
α1
α2
α3
下列说法正确的是
A.2 c1>c3 B.a + b=92.4 C.2P1<P3 D.α1 +α3=1
高三化学单选题困难题查看答案及解析
-
(9分)在一定温度下, 把2molN2和6molH2通入体积不变的容器中。容器中发生以下反应: N2(g) + 3H2(g)
2NH3(g) ,△H= —QKJ/mol。若反应达平衡后, 测得混合气体为7mol。据此回答下列问题:
保持上述反应温度不变, 设a.b.c分别代表起始加入的N2.H2和NH3的物质的量。如果反应达平衡后混合气体中各物质的百分含量仍与上述平衡时完全相同, 那么:
(1)若a = 1.c =" 2," 则b =________。在此情况下, 反应起始时将向________方向进行(填“正”或“逆”)。
(2)若需规定起始时反应向逆方向进行,则c的范围是________。
高三化学填空题中等难度题查看答案及解析
-
氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g) + 3H2(g)
2NH3(g);ΔH = -92.2 kJ·mol-1。
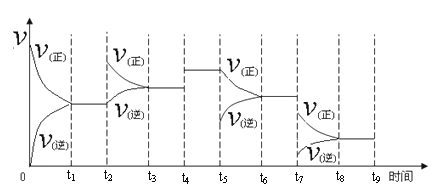
① 一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5 ﹑t7时刻所对应的实验条件改变分别是
t4 ________t5 ________ t7________。
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为________。
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g)
H2(g) + CO(g) △H = +131.3 kJ/mol
①该反应在低温下不能自发进行的原因是________。
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度 ( )
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol碘化氢(a>b)待反应:2HI(g)
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A________c(I2)B ;平衡时HI的分解率αA________αB ;平衡时H2在混合气体中的体积分数A________B (填写“>”“<”“=”)
高三化学填空题中等难度题查看答案及解析
-
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下[已知N2(g)十3H2(g)
2NH3(g) △H=-92.4kJ/mol];下列说法正确的是( )
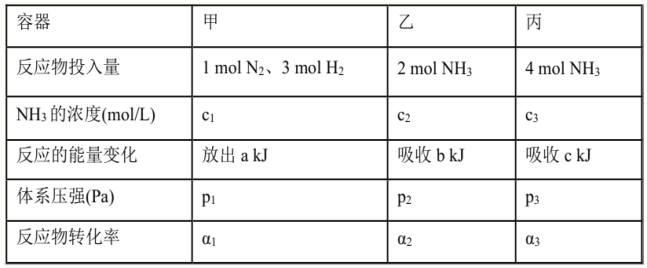
A. 2c1>c3 B. a+b>92.4 C. 2p2<p3 D. α1+α3<1
高三化学单选题困难题查看答案及解析
-
在容积固定不变的密闭容器中加入1mol N2和3mol H2发生反应:N2(g)+3H2(g)
2NH3(g) △H= —92.4 kJ·mol-1,下列结论正确的是
A.该反应达到平衡时,放出的热量等于92.4kJ
B.达到平衡后向容器中通入1mol氦气,平衡不移动
C.降低温度和缩小容器体积均可使该反应的平衡常数增大
D.若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的90%
高三化学选择题简单题查看答案及解析
-
在容积不变的密闭容器中,分别充入1.0 mol N2和3.0 mol H2,在不同温度下,任其发生反应:N2(g)+3H2(g)
2NH3(g)。分别在同一时刻,不同温度下测定NH3的含量,然后绘制出如下图所示的曲线。
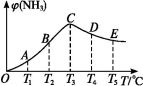
请回答下列问题:
(1)A、B、C、D、E五点中,尚未达到平衡状态的是 。
(2)此可逆反应的正反应是 (填“放热”或“吸热”)反应。
(3)AC段的曲线是增函数,CE段的曲线是减函数,试从反应速率和化学平衡的角度说明理由: 。
高三化学填空题中等难度题查看答案及解析
-
(10分)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)
2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
⑴ 根据下图,计算从反应开始到平衡时,平均反应速率v(NH3)=______________________________
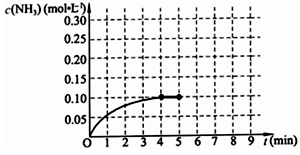
⑵ 该反应450℃的平衡常数________500℃时的平衡常数(填“>”、“<”或“=”)。
⑶ 下列描述中能说明上述反应已达平衡的是___________。
A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
⑷ 第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡_______________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
⑸ 第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3浓度约为0.25mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
高三化学填空题简单题查看答案及解析
-
(10分)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)
2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
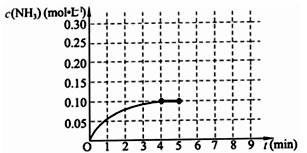
⑴ 根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)=_________________。
⑵ 该反应450℃的平衡常数________500℃时的平衡常数(填“>”、“<”或“=”)。
⑶ 下列描述中能说明上述反应已达平衡的是___________。
A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
⑷ 第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡_______________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
⑸ 第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3浓度约为0.25mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
高三化学填空题简单题查看答案及解析