对于敞口容器中化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ,下列叙述不正确的是 ( )

A、反应过程中能量关系可用上图表示
B、Zn和H2SO4的总能量大于ZnSO4和H2的总能量
C、若将该反应设计成原电池,锌为负极
D、若将其设计为原电池,当有32.5g锌溶解时,正极要放出11.2L气体
高三化学选择题简单题
对于敞口容器中化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ,下列叙述不正确的是 ( )

A、反应过程中能量关系可用上图表示
B、Zn和H2SO4的总能量大于ZnSO4和H2的总能量
C、若将该反应设计成原电池,锌为负极
D、若将其设计为原电池,当有32.5g锌溶解时,正极要放出11.2L气体
高三化学选择题简单题
对于敞口容器中化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ,下列叙述不正确的是 ( )

A、反应过程中能量关系可用上图表示
B、Zn和H2SO4的总能量大于ZnSO4和H2的总能量
C、若将该反应设计成原电池,锌为负极
D、若将其设计为原电池,当有32.5g锌溶解时,正极要放出11.2L气体
高三化学选择题简单题查看答案及解析
已知Zn(s)+ H2SO4(aq)= ZnSO4(aq)+ H2(g) ΔH<0;则下列叙述不正确的是
A.该反应的ΔH值与反应物用量无关
B.该反应的化学能可以转化为电能
C.反应物的总能量高于生成物的总能量
D.该反应中反应物的化学键断裂放出能量,生成物化学键形成吸收能量
高三化学选择题中等难度题查看答案及解析
对于Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g)的化学反应(反应放热),下列叙述一定正确的是( )
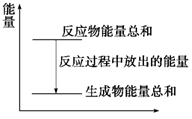
A.反应过程中的能量关系可用上图表示
B.1 mol锌的能量高于1 mol H2所含的能量
C.若将该反应设计成原电池,锌为负极
D.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L
高三化学选择题简单题查看答案及解析
对于化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g);△H=a kJ/mol,下列叙述不正确的是( )
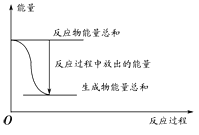
A. 反应过程中能量关系如上图表示,则该反应为放热反应
B. 若将该反应设计成原电池,锌为负极
C. 化学反应的焓变与反应方程式的计量数有关
D. 若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L
高三化学单选题中等难度题查看答案及解析
对于反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g),下列叙述不正确的是( )
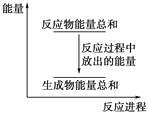
A.其反应物或生成物都能用来表示该反应的速率
B.反应过程中能量关系可用上图表示
C.若将该反应设计成原电池,锌为负极
D.若设计为原电池,当有32.5 g锌溶解,标准状况下正极放出11.2 L气体
高三化学单选题中等难度题查看答案及解析
已知Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ΔH<0;则下列叙述不正确的是( )
A.该反应的ΔH值与反应物用量无关
B.该反应的化学能可以转化为电能
C.反应物的总能量高于生成物的总能量
D.该反应中反应物的化学键断裂放出能量,生成物化学键形成吸收能量
高三化学选择题中等难度题查看答案及解析
H2O(g)―→H2O(l)是一个放热过程,但不是化学反应,A错。HI+H2SO4(aq)=ZnSO4(aq)+H2(g) ΔH<0,则下列关于该反应的叙述不正确的是 ( )
A.该反应中旧键断裂需吸收能量,新键形成需放出能量,所以总能量不变
B.上述热化学方程式中的ΔH的值与反应物的用量无关
C.该反应的化学能可以转化为电能
D.反应物的总能量高于生成物的总能量
高三化学选择题中等难度题查看答案及解析
下列有关热化学方程式书写及对应表述均正确的是
A. 浓H2SO4与0.1 mol·L-1NaOH反应:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
B. 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热充分反应,放出19.12 kJ热量。则Fe(s)+S(s)===FeS(s) ΔH=-95.6 kJ·mol-1
C. 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)===2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1
D. 已知2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1,则可知C的燃烧热ΔH=-110.5 kJ·mol-1
高三化学单选题中等难度题查看答案及解析
下列变化中生成物的总能量大于反应物的总能量的是
A.H—Cl→H + Cl B.H + H→H—H
C.Zn + H2SO4 = ZnSO4 + H2 ↑ D.HCl+ NaOH = NaCl+ H2O
高三化学选择题简单题查看答案及解析
高三化学选择题中等难度题查看答案及解析