-
用铝热法还原下列化合物,制得金属1mol,消耗铝最少的是( )
A. MnO2 B. WO3 C. Co3O4 D. Cr2O3
高三化学单选题简单题查看答案及解析
-
用铝热法还原下列氧化物,制得金属各1mol,消耗铝最少的是( )
A.MnO2
B.WO3
C.Cr2O3
D.Co3O4高三化学选择题中等难度题查看答案及解析
-
用铝热法还原下列氧化物制得金属各1 mol,消耗铝最少的是
A.MnO2 B.WO3 C.Cr2O3 D.Co3O4
高三化学选择题中等难度题查看答案及解析
-
用铝热法还原下列化合物,制取金属1mol,消耗铝最少的是( )
A.MnO2 B.WO3 C.Co3O4 D.Cr2O3
高三化学选择题简单题查看答案及解析
-
用铝热法还原下列物质,制得金属各1mol,消耗铝最少的是( )
A.MnO2 B.Fe3O4 C.Cr2O3 D.V2O5
高三化学选择题中等难度题查看答案及解析
-
锰及其化合物在现代工业及国防建设中具有十分重要的意义。回答下列问题:
(1)常用铝热法还原软锰矿(主要成分为MnO2)来制金属锰。因为铝和软锰矿反应剧烈,所以先在强热条件下将软锰矿变为Mn3O4,然后再将其与铝粉混合。
①MnO2中Mn的化合价为________________。
②铝粉与Mn3O4反应时,还原剂与氧化剂的物质的量之比为_________________。
(2)pH=0的溶液中,不同价态锰的微粒的能量(△G)如图所示,若某种含锰微粒(如Mn3+)的能量处于相邻价态两种微粒(Mn2+和MnO)能量连线的上方,则该微粒不稳定,会发生歧化反应,转化为相邻价态的微粒。
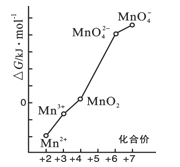
①MnO42-_________________(填“能”或“不能”)稳定存在于pH=0的溶液中。
②实验室可利用以下反应检验Mn2+的存在:2Mn2++5S2O82-+8H2O=16H++10SO42-+2MnO4-,确认Mn2+存在的现象是__________________;检验时必须控制Mn2+的浓度和用量,否则实验失败。理由是___________________________________。
高三化学综合题简单题查看答案及解析
-
锰及其化合物在现代工业及国防建设中具有十分重要的意义。回答下列问题:
(1)常用铝热法还原软锰矿(主要成分为MnO2)来制金属锰。因为铝与软锰矿反应剧烈,所以先在强热条件下将软锰矿转变为Mn3O4,然后再将其与铝粉混合。
①MnO2中Mn的化合价为____________________。
②铝粉与Mn3O4反应时,还原剂与氧化剂的物质的量之比为_________________。
(2)pH=0的溶液中,不同价态锰的微粒的能量(E)如图所示。若某种含锰微粒(如Mn3+)的能量处于相邻价态两种微粒(Mn2+和MnO2)能量连线的上方,则该该微粒不稳定,会发生歧化反应,转化为相邻价态的微粒。
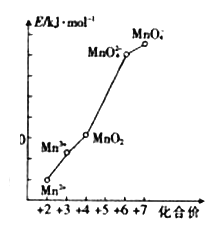
①MnO42-______(填“能”或“不能”)稳定存在于pH=0的溶液中。
②实验室可利用以下反应检验Mn2+的存在:2Mn2++5S2O82-+8H2O==16H++10SO42-+2 MnO42-,确认Mn2+存在的现象是______________________;检验时必须控制Mn2+的浓度和用量,否则实验失败,理由是___________________________________。
高三化学简答题简单题查看答案及解析
-
金属钨用途广泛,H2还原WO3可得到钨,其总反应为:WO3+3H2
W+3H2O,该总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如表所示,假设WO3完全转化为W,则三个阶段消耗H2质量之比为
温度(℃)
25℃~550℃~600℃~700℃
主要成分
WO3 W2O5 WO2 W
A.1:1:4 B.1:1:3 C.1:1:2 D.1:1:1
高三化学单选题中等难度题查看答案及解析
-
下列说法中不正确的是( )
A. 在金属的冶炼方法中,铝热法,本质上属于热还原法
B. 化学上所说的钢铁,其实钢是钢,铁是铁,钢是混合物,而铁是纯净物
C. 对于反应:FeCuS2 + S
FeS2 + CuS,其中FeS2既是氧化产物又是还原产物
D. 已知BrCl的化学性质跟Cl2相似,则BrCl跟水反应(生成HCl和HBrO)也是氧化还原反应
高三化学选择题中等难度题查看答案及解析
-
下列说法中不正确的是( )
A. 在金属的冶炼方法中,铝热法,本质上属于热还原法
B. 化学上所说的钢铁,其实钢是钢,铁是铁,钢是混合物,而铁是纯净物
C. 对于反应:FeCuS2 + S
FeS2 + CuS,其中FeS2既是氧化产物又是还原产物
D. 已知BrCl的化学性质跟Cl2相似,则BrCl跟水反应(生成HCl和HBrO)也是氧化还原反应
高三化学选择题中等难度题查看答案及解析