-
乙二胺(H2NCH2CH2NH2),无色液体,有类似于氨的性质 ,已知:25℃时,电离常数kb1=10-4.07 kb2=10-7.15;乙二胺溶液中各含氮微粒的分布分数δ(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液pH的变化曲线如右图。下列说法错误的是( )
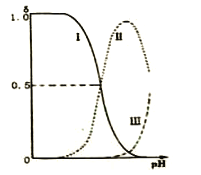
A. H2NCH2CH2NH2在水溶液中第一步电离的方程式H2NCH2CH2NH2+H2O H2NCH2CH2NH3++OH-
H2NCH2CH2NH3++OH-
B. 曲线Ⅰ代表的微粒符号为[H3NCH2CH2NH3]2+
C. 曲线Ⅰ与曲线Ⅱ相交点对应pH=4.07
D. 在0.1 mol·L-1 H2NCH2CH2NH3Cl溶液中各离子浓度大小关系为c(Cl-)>c(H2NCH2CH2NH3+)>c(H+)>c(OH-)
-
乙二胺(H2NCH2CH2NH2),无色液体,有类似氨的性质。已知:25℃时,Kb1=10-4.07Kb2=10-7.15;乙二胺溶液中各含氮微粒的分布分数δ(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液pH的变化曲线如右图。下列说法错误的是
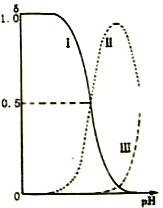
A. H2NCH2CH2NH2在水溶液中第一步电离的方程式为:H2NCH2CH2NH2+H2O H2NCH2CH2NH3++OH-
H2NCH2CH2NH3++OH-
B. 曲线Ⅰ代表的微粒符号为[H3NCH2CH2NH3]2+
C. 曲线Ⅰ与曲线Ⅱ相交点对应pH=4.07
D. 在0.1mol·L-1 H2NCH2CH2NH3Cl溶液中各离子浓度大小关系为c(Cl-)>(H2NCH2CH2NH3+) >c(OH-)>c(H+)
-
乙二胺(H2NCH2CH2NH2),无色液体,电离类似于氨:NH3+H2O NH4++OH-,25℃时,kb1=10-4.07,kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是
NH4++OH-,25℃时,kb1=10-4.07,kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是
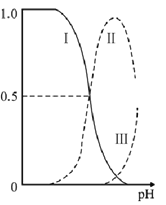
A. 曲线Ⅱ代表的微粒符号为H2NCH2CH2NH3+
B. 曲线Ⅰ与曲线II相交点对应pH=6.85
C. 0.1 mol ·L-1H2NCH2CH2NH3Cl溶液中各离子浓度大小关系为c(Cl-)>c(H2NCH2CH2NH3+)>c(H+)>c(OH-)
D. 乙二胺在水溶液中第二步电离的方程式H2NCH2CH2NH3++H2O [H3NCH2CH2NH3]2++OH-
[H3NCH2CH2NH3]2++OH-
-
乙二胺(H2NCH2CH2NH2)是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是( )
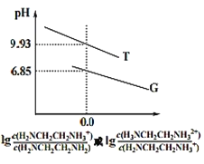
A.Kb2[H2NCH2CH2NH2]的数量级为10-8
B.曲线G代表pH与lg 的变化关系
的变化关系
C.H3NCH2CH2NH2Cl溶液中c(H+)>c(OH-)
D.0.01mol·L-1H2NCH2CH2NH2电离度约为10%
-
乙二胺(H2NCH2CH2NH2 )是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是
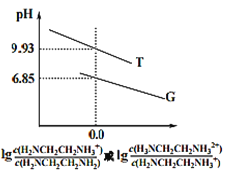
A. Kb2[H2NCH2CH2NH2] 的数量级为10-8
B. 曲线G代表pH 与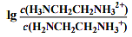 的变化关系
的变化关系
C. H3NCH2CH2NH2Cl溶液中c(H+)>c(OH-)
D. 0.01mol·L-1H2NCH2CH2NH2 电离度约为10%
-
已知二元弱碱B(OH)2在水中存在如下电离平衡:B(OH)2  B(OH)++OH-,Kb1=10-3.75;B(OH)+
B(OH)++OH-,Kb1=10-3.75;B(OH)+ B2++OH-,Kb2=10-7.62。常温下,用0.1 mol/L盐酸滴定25 mL 0.1 mol/L的B(OH)2溶液,得到如图所示的滴定曲线。下列说法不正确的是
B2++OH-,Kb2=10-7.62。常温下,用0.1 mol/L盐酸滴定25 mL 0.1 mol/L的B(OH)2溶液,得到如图所示的滴定曲线。下列说法不正确的是

A. a点所得的溶液中:c[B(OH)2]= c[B(OH)+]
B. b点所得的溶液中:c[B(OH)2] +c(OH-)=c(B2+)+c(H+)
C. c点所得的溶液中:c(Cl-)<3c[B(OH)+]
D. d点所得的溶液中:c(B2+)>c[B(OH)+]>c[B(OH)2]
-
乙二胺(H2NCH2CH2NH2 )是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是

A. 常温下,pKb2=-1gKb2 =7.15
B. 溶液中水的电离程度:a点大于b点
C. H3NCH2CH2NH2Cl2 溶液中c(H+)>c(OH-)
D. 曲线G代表pH 与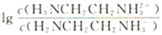 的变化关系
的变化关系
-
甲酸(化学式HCOOH,分子式CH2O2,相对分子质量46),俗名蚁酸,是最简单的羧酸,无色而有刺激性气味的易挥发液体。熔点为8.6 ℃,沸点100.8℃,25℃电离常数Ka=1.8×10-4。某化学兴趣小组进行以下实验。
Ⅰ.用甲酸和浓硫酸制取一氧化碳
A. 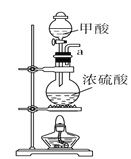 B.
B. 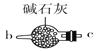 C.
C. 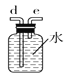 D.
D. 
(1)请说出图B中盛装碱石灰的仪器名称__________。用A图所示装置进行实验。利用浓硫酸的脱水性,将甲酸与浓硫酸混合,甲酸发生分解反应生成CO,反应的化学方程式是________;实验时,不需加热也能产生CO,其原因是_______。
(2)如需收集CO气体,连接上图中的装置,其连接顺序为:a→__________(按气流方向,用小写字母表示)。
Ⅱ.对一氧化碳的化学性质进行探究
资料:ⅰ.常温下,CO与PdCl2溶液反应,有金属Pd和CO2生成,可用于检验CO;
ⅱ.一定条件下,CO能与NaOH固体发生反应:CO+NaOH HCOONa
HCOONa
利用下列装置进行实验,验证CO具有上述两个性质。
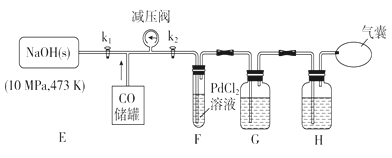
(3)打开k2,F装置中发生反应的化学方程式为_____________;为了使气囊收集到纯净的CO,以便循环使用,G装置中盛放的试剂可能是_________,H装置的作用是____________。
(4)现需验证E装置中CO与NaOH固体发生了反应,某同学设计下列验证方案:取少许固体产物,配置成溶液,在常温下测该溶液的pH,若pH>7,证明CO与NaOH固体发生了反应。该方案是否可行,请简述你的观点和理由:________,_________。
(5)25℃甲酸钠(HCOONa)的水解平衡常数Kh的数量级为____________。若向100ml 0.1mol.L-1的HCOONa溶液中加入100mL0.2mol.L-1的HCl溶液,则混合后溶液中所有离子浓度由大到小排序为_________。
-
图(1)和图(2)分别为二元酸H2A和乙二胺(H2NCH2CH2NH2)溶液中各微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线(25℃)。下列有关说法正确的是
已知:H2NCH2CH2NH2+H2O [H3NCH2CH2NH2]++OH-
[H3NCH2CH2NH2]++OH-
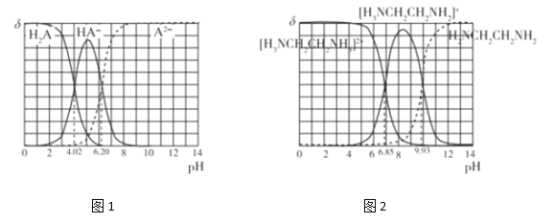
A. [H3NCH2CH2NH3]A溶液显碱性
B. NaHA溶液中各离子浓度大小关系为:c(Na+)>c(HA-)>c(OH-)>c(A2-)>(H+)
C. 乙二胺(H2NCH2CH2NH2)的Kb2=10-7.15
D. 向[H3NCH2CH2NH2][HA]溶液中通入一定量的HCl气体,则c(H2NCH2CH2NH2)c(H2A)/[c([H2NCH2CH2NH3]+)c(HA-)]可能增大也可能减小
-
常温下,H2A和H2NCH2CH2NH2溶液中各组分的物质的量分数δ随pH的变化如图(I)、(II)所示。下列说法不正确的是已知: 。
。
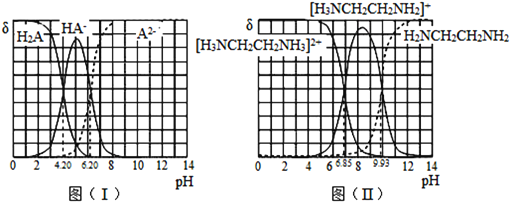
A.NaHA溶液中各离子浓度大小关系为:
B.乙二胺(H2NCH2CH2NH2)的Kb2=10-7.15
C.[H3NCH2CH2NH3]A溶液显碱性
D.向[H3NCH2CH2NH2] HA溶液中通人HCl,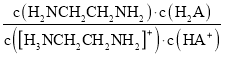 不变
不变

H2NCH2CH2NH3++OH-




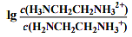 的变化关系
的变化关系

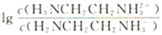 的变化关系
的变化关系 B.
B.  C.
C.  D.
D. 


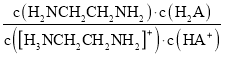 不变
不变