-
某化学兴趣小组进行以下实验探究:
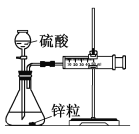
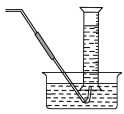
Ⅰ. 设计实验探究反应速率的测定和比较
实验步骤:
(1)取一套装置(装置如图所示),加入40 mL 1 mol·L-1的硫酸,测量收集10 mL H2所需的时间。
(2)取另一套装置,加入40 mL 4 mol·L-1的硫酸,测量收集10 mL H2所需的时间。
实验现象: 锌跟硫酸反应产生气泡,收集10 mL气体,(2)所用时间比(1)所用时间________(填“长”或“短”);
实验结论: 4 mol·L-1硫酸与锌反应比1 mol·L-1硫酸与锌反应速率______(填“大”或“小”)。
注意事项:① 锌粒的颗粒(即表面积)大小________________;
② 40 mL的硫酸要迅速加入;
③ 装置____________________,且计时要迅速准确;
④ 气体收集可以用排水量气装置代替。
实验讨论:除本实验测定反应速率的方法外,可行的方案还有(任写一种)
________________________________________________________________。
Ⅱ. 探究用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素,所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K。
请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T(K) | 大理石规格 | HNO3浓度 (mol·L-1) | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (1)实验①和②探究HNO3浓度对该反应速率的影响 (2)实验①和_____探究温度对该反应速率的影响 (3)实验①和_____探究大理石规格(粗、细)对该反应速率的影响 |
| ② | _____ | ________ | _________ |
| ③ | _____ | 粗颗粒 | _________ |
| ④ | ______ | ______ | ________ |
-
某化学兴趣小组设计实验探究反应速率的测定和比较。
[实验步骤]
Ⅰ.取一套装置(装置如下图所示),加入40mL1mol/L的硫酸,测量收集10mLH2所需的时间。
Ⅱ.取另一套装置,加入40mL1mol/L的硫酸,测量收集10mLH2所需的时间。
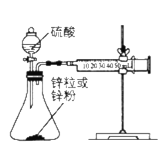
(1)[实验现象]
锌跟硫酸反应产生气泡,收集10mL气体, Ⅱ所用时间比Ⅰ所用时间_____。
(2)[实验结论]
4mol/L硫酸与锌反应比1mol/L硫酸与锌反应速率____。
(3)[注意事项]
a.锌粒的颗粒(即表面积)大小_____;
b.40mL硫酸要迅速加入;
c.装置____,且计时要迅速、准确;
d.气体收集可以用排水量气装置代替。
(4)实验讨论]除本实验测定反应速率的方法外,可行的方案还有(填两条):
a.________;b._______。
-
某化学兴趣小组设计实验探究反应速率的测定和比较。
【实验目的】测定锌与稀硫酸反应的速率
【实验用品】锥形瓶、双孔塞、胶皮管、分液漏斗、直角导管、50mL注射器、铁架台、秒表、锌粒、1 mol/L硫酸、4 mol/L硫酸。
【实验步骤】
(1)取一套装置(如图所示),加入40 mL 1 mol/L的硫酸和锌粒,测量收集10 mL H2所需的时间。
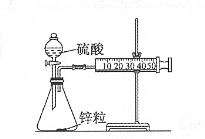
(2)取另一套装置,加入40 mL4 mol/L的硫酸和锌粒,测量收集10 mL H2所需的时间。
【实验现象】锌与稀硫酸反应 (写现象),收集10mL气体,(2)所用时间比(1)所用时间_________。
【实验结果】
| 加入试剂 | 反应时间 | 反应速率 |
| 40 mL 1 mol/L硫酸 | 长 | _________ |
| 40 mL 4 mol/L硫酸 | 短 | _________ |
【实验结论】4 mol/L硫酸与锌反应比1 mol/L硫酸与锌反应的速率 。
【注意事项】(1)锌的颗粒(即表面积)大小 ;
(2)40 mL的硫酸要迅速加入;
(3)装置 ,且计时要迅速准确;
(4)气体收集可以用排水量气装置(如图所示)代替。

【实验讨论】除本实验测定反应速率的方法外,可行的方案还有(至少填两种):
(1) 。
(2) 。
-
某化学兴趣小组,拟探究和比较SO2和C12的化学性质,设计如图所示的实验装置二套。请你参与探究并回答下列问题。
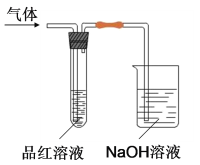
(1)向第一套装置中通入一段时间的SO2,观察到试管中的品红溶液________(填“褪色”或“不褪色”),然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(2)向第二套装置中通入一段时间的C12,观察到试管中的品红溶液也褪色,然后再加热试管,溶液_________,(填“恢复”或“不恢复”)红色;
(3)由以上两个实验可以说明SO2和C12的漂白原理________(填“相同”或“不相同”)。 完成化学方程式C12 + H2O ==_______________________。
-
甲、乙两个实验小组利用 酸性溶液与
酸性溶液与 溶液反应研究影响反应速率的因素。
溶液反应研究影响反应速率的因素。
设计实验方案如下 实验中所用
实验中所用 溶液均已加入
溶液均已加入 :
:
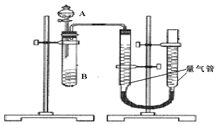
甲组:通过测定单位时间内生成 气体体积的大小来比较化学反应速率的大小某同学进行实验,实验装置如图.其中A、B的成分见表
气体体积的大小来比较化学反应速率的大小某同学进行实验,实验装置如图.其中A、B的成分见表
| 序号 | A溶液 | B溶液 |
| ① |  溶液 溶液
|  溶液 溶液
|
| ② |  溶液 溶液
|  溶液 溶液
|
| ③ |  溶液 溶液
|  溶液和少量 溶液和少量
|
 该反应的离子方程式为 ______
该反应的离子方程式为 ______
 实验开始前需要检查气密性.分液漏斗中A溶液应该 ______ 加入
实验开始前需要检查气密性.分液漏斗中A溶液应该 ______ 加入 填“一次性”或“逐滴滴加”
填“一次性”或“逐滴滴加”
 完成该实验还需要 ______
完成该实验还需要 ______  填仪器名称
填仪器名称 ,实验结束后读数前需要移动量气管,使两个量气管的液面相平.
,实验结束后读数前需要移动量气管,使两个量气管的液面相平.
乙组:通过测定 溶液褪色所需时间的多少来比较化学反应速率为了探究
溶液褪色所需时间的多少来比较化学反应速率为了探究 与
与 浓度对反应速率的影响,某同学在室温下完成以下实验
浓度对反应速率的影响,某同学在室温下完成以下实验
| 实验编号 | 1 | 2 | 3 | 4 |
| 水 | 10 | 5 | 0 | X |
| 
| 5 | 10 | 10 | 5 |
| 
| 5 | 5 | 10 | 10 |
| 时间 | 40 | 20 | 10 | --- |
 ______ ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 ______ 。
______ ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 ______ 。
 号反应中,
号反应中, 的反应速率为 ______。
的反应速率为 ______。
 在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
| 时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 温度℃ | 25 | 26 | 26 | 26 | 
| 27 | 27 |
结合实验目的与表中数据,你得出的结论是 ______。
 从影响化学反应速率的因素看,你的猜想还可能是 ______ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 ______
从影响化学反应速率的因素看,你的猜想还可能是 ______ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 ______  填字母
填字母 。
。
A 硫酸钾  水
水  二氧化锰
二氧化锰  硫酸锰。
硫酸锰。
-
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:甲同学利用Al、Fe、Mg和2 mol/L的稀硫酸,设计实验方案研究影响反应速率的因素。
研究的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol/L的硫酸于试管中;②分别投入大小、形状相同的Al、Fe、Mg | 反应快慢:Mg>Al>Fe | 反应物的性质越活泼,反应速率越快 |
(1)该同学的实验目的是_______________________;要得出正确的实验结论,还需控制的实验条件是________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置同温下进行定量实验,用大小形状相同的Fe分别和0.5 mol/L及2 mol/L的足量稀H2SO4反应,通过________可以说明浓度对化学反应速率的影响。
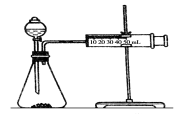
实验二:同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(s,白磷)+5O2(g)===P4O10(s) ΔH1=-2983.2 kJ·mol-1①
P(s,红磷)+5/4O2(g)===1/4 P4O10(s) ΔH2=-738.5 kJ·mol-1②
则白磷转化为红磷的热化学方程式为 。相同状况下,能量状态较低的是________;白磷的稳定性比红磷________(填“高”或“低”)。)
-
(题文)某兴趣小组设计了如图所示装置(部分夹持装置已略去)进行实验探究。
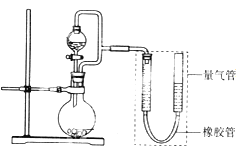
(实验一)探究影响化学反应速率的因素。
圆底烧瓶中装锌片(两次实验中所用锌片大小和外形相同)、恒压分液漏斗中装稀硫酸,以生成20.0mL气体为计时终点,结果为t1>t2。
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 3 | t2 |
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s | |
| I | 40 | 1 | t1 | |
| II | 40 | 3 | t2 | |
| | | | | | | |
检查该装置气密性的方法是_______________________________________________。
比较实验I和Ⅱ可以得出的结论是____________________________________________。
(实验二)探究铁的电化学腐蚀。
①圆底烧瓶中装铁粉和碳粉混合物,恒压分液漏斗中装稀硫酸,打开活塞加入稀硫酸后量气管中出现的现象是:左侧液面_________右侧液面_________(选填“上升”、“下降”)。
②圆底烧瓶中装与①相同量的铁粉但不加入碳粉,其他试剂和操作相同,发现左、右侧液面变化较_______(选填“快”、“慢”,下同),说明原电池反应比一般化学反应_______。
③圆底烧瓶中装与①相同量的铁粉和碳粉混合物,恒压分液漏斗中装食盐水,打开活塞加入食盐水后,你预测量气管中出现的现象是:___________________________________,正极的电极反应是___________________________。
-
为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
实验一:
利用如图装置测定化学反应速率(已知:S2O32-+2H+═H2O+S↓+SO2↑)

(1)除如图装置所示的实验用品外,还需要的一种实验用品是________。
A.温度计 B.秒表 C.酒精灯
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是__________。
实验二:
为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表。(已知 I2+2S2O32-═S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s |
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 |
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
(3)表中Vx=____mL,t1、t2、t3的大小关系是________。
实验三:
取5mL0.1mol/L的KI溶液于试管中,滴加0.1 mol·L-1 FeCl3溶液溶液2mL,发生如下反应:2Fe3++2I-==2Fe2++I2.为证明该反应达到一定可逆性且具有限度,他们设计了如下实验:
①取少量反应液,滴加AgNO3溶液,发现有少量黄色(AgI)沉淀;
②再取少量反应液,滴加少量CCl4,振荡,发现CCl4层显浅紫色.
根据①②的现象,他们得出结论:该反应具有一定的可逆性,在一定条件下会达到反应限度.
(4)指导老师指出他们上述实验中①不合理,你认为其原因是__________;改进的方法是_______。
(5)有人认为步骤②适合检验生成I2较多的情况下,还有一种简便方法可以灵敏地检验是否生成了I2,这种方法所用的试剂是____________________。
-
某化学兴趣小组,拟探究和比较SO2和C12的漂白性,设计如下图所示的实验装置二套。请你参与探究并回答下列问题。
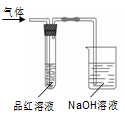
(1)向第一套装置中通入一段时间的SO2,观察到试管中的品红溶液 (填“能”或“不能” )褪色,然后再加热试管,溶液 (填“恢复”或“不恢复”)红色;
(2)向第二套装置中通入一段时间的C12,观察到试管中的品红溶液也褪色,然后再加热试管,溶液 (填“恢复”或“不恢复”)红色;
(3)由以上两个实验可以说明SO2和C12的漂白原理 (填“相同”或“不相同”);
(4) C12通入品红溶液中,生成的具有漂白性的物质是 (填“HC1”或“HClO”)。
-
某化学兴趣小组,拟探究和比较SO2和C12的漂白性,设计如下图所示的实验装置二套。请你参与探究并回答下列问题。
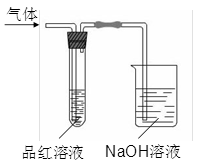
(1)向第一套装置中通入一段时间的SO2,观察到试管中的品红溶液褪色,然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(2)向第二套装置中通入一段时间的C12,观察到试管中的品红溶液也褪色,然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(3)由以上两个实验可以说明SO2和C12的漂白原理________(填“相同”或“不相同”);
(4) C12通入品红溶液中,生成的具有漂白性的物质是________(填“HC1”或“HClO”)。











