-
H2O2既可以作氧化剂,又可以作还原剂。现在H2O2溶液中加入用硫酸酸化的KMnO4溶液,紫红色的KMnO4溶液变成了无色溶液。该反应体系中共七种物质:O2、KMnO4、MnSO4、H2SO4、K2SO4、H2O、H2O2。
(1)请将以上反应物与生成物分别填入以下空格内___。

(2)该反应中的还原剂是__(填化学式)被还原的元素是____(填元素符号)。
(3)如反应中电子转移了0.5mol,则产生的气体在标准状况下的体积为__L。
(4)+6价铬的化合物毒性较大,酸性溶液中常用NaHSO3将废液中的Cr2O72-还原成Cr3+,该反应的离子方程式为___。
高三化学填空题中等难度题查看答案及解析
-
现有下列10种物质:①Na2CO3 ②AlCl3 ③HCl ④NH4HCO3 ⑤C2H5OH ⑥Al ⑦食盐水 ⑧石墨 ⑨冰醋酸 ⑩二氧化碳
(1)上述物质中属于强电解质的是__;属于非电解质的是__;能导电的是__。(填序号)
(2)既能跟盐酸反应又能跟NaOH溶液反应的是__(填序号)。
高三化学填空题简单题查看答案及解析
-
碱式碳酸镍[Nix(OH)y(CO3)z·nH2O]是一种绿色晶体,常用作催化剂和陶瓷着色剂,为确定其组成,某小组进行了实验探究。
(查阅资料)碱式碳酸镍300℃以上时分解生成3种氧化物。NiO为绿色粉末,Ni2O3为灰黑色固体。
(实验探究)选用下图所示部分装置进行实验(夹持装置略)
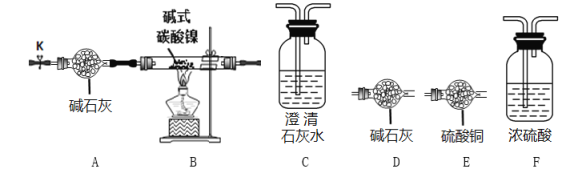
实验I定性探究:确定3种氧化物的组成。
(1)预测三种氧化物分别是含Ni、H、、C三种元素的理论依据是___________________。
(2)经检验生成的三种氧化物分别为NiO、H2O和CO2,装置连接顺序为AB__________(填装置的字母序号)。其中装置B现象为_________________。
实验II 定量确定碱式碳酸镍的组成。连接装置A-B-F-D-D进行实验。
实验步骤如下:
i 称量碱式碳酸镍、装置F、装置D(前一个)的质量并记录
ii 打开活塞K,缓缓通入空气
iii点燃酒精灯,加热
iv熄灭酒精灯, 冷却到室温, 关闭K
v 再次称量装置F、装置D(前一个)的质量并记录
(3)其中步骤ii的目的是_____________________________________。
(4)若缺少装置A将导致所测得的x值___________(填“偏大”或“偏小”或“无影响”)。
(5)重复操作ii-v至__________________________时,可判断碱式碳酸镍已完全分解。
(6)实验前测得石英玻璃管中的样品质量为3.77g,其他数据如下表所示
装置F质量/g
装置D(前一个)质量/g
实验前
132.00
41.00
实验后
133.08
41.44
该碱式碳酸镍的化学式为____________________________________。
高三化学填空题中等难度题查看答案及解析
-
已知亚磷酸(H3PO3)的结构如图,
是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式____。亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为____。
(2)某温度下,0.1mol/L的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2mol/L该温度下H3PO3的一级电离平衡常数
=____。(H3PO3第二步电离忽略不计,结果保留两位有效数字)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:
____
(填“>”、“<”或“=”)。
高三化学填空题中等难度题查看答案及解析
-
三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
对于反应2SiHCl3(g)=SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。
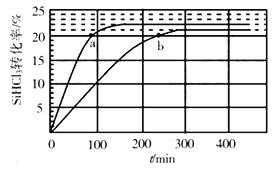
①343K时反应的平衡转化率α=___%。平衡常数K343K=__(保留2位小数)。
②在343K下:要提高SiHCl3转化率,可采取的措施是__;要缩短反应达到平衡的时间,可采取的措施有___、___。
③比较a、b处反应速率大小:va___vb(填“大于”“小于”或“等于”)。反应速率v=v正-v逆=
-
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处
=___(保留1位小数)。
高三化学填空题困难题查看答案及解析
-
钛及其化合物应用广泛。
(1)(钛元素基态原子核外最外层电子的自旋状态___(填“相同”或“相反”)。
(2)已知一定条件下TiO2与TiCl4之间可以相互转化:TiO2
TiCl4。
①Ti、Cl、O三种元素电负性由大到小的顺序为___。
②COCl2的分子构型为___,键角大小比较∠Cl—C—O___∠C1—C—Cl(填“>”或“<”),σ键和π键数目之比为___。
③已知室温下TiCl4为无色易溶于乙醇的液体,则TiCl4的晶体类型为___。
(3)配合物[TiCl(H2O)5]Cl2·H2O中,中心离子的配位数是___,向1mol该配合物中加入足量AgNO3溶液,可以得到___molAgCl沉淀。
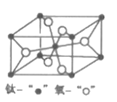
(4)金红石型TiO2的晶胞(α=β=γ=90o)如图所示:TiO2晶体中O原子的配位数是___,其晶胞参数为:a=b=459pm,c=295pm,该晶体密度为___g/cm3(列出计算式)。
高三化学填空题中等难度题查看答案及解析
-
过氧乙酸又名过醋酸
,是重要化工原料,也是一种绿色生态杀菌剂,其制法为
。
(1)某同学写出了碳原子的4种不同状态的电子排布图:
a.
b.
c.
d.
其中能量最低的是________(填标号),电子由状态C到状态B所得到的光谱为________光谱(填“原子发射”或“原子吸收”)。
(2)过氧乙酸分子中C原子的杂化方式有________。
(3)乙酸比乙醇易电离出
的原因____________________。
(4)熔点:乙酸________硝酸(填“>”、“<”或“=”),理由_________________。
(5)造纸中,用
与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
①两种硼氢化物的熔点如下表所示:
硼氢化物
熔点/℃
400
-64.5
解释表中两种物质熔点差异的原因________。
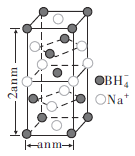
②硼氢化钠晶胞结构如图所示,该晶体中
的配位数为________。已知:硼氢化钠晶体的密度为
,
代表阿伏伽德罗常数的值,则a=________nm(用含
、
的最简式子表示)。
高三化学填空题困难题查看答案及解析
-
烟气中SO2和NOx(NO及NO2)的脱除对于环境保护意义重大。
(1)湿式氨法烟气脱硫脱氮是通过氨水吸收烟气,得到含
、
、
、
和NO2的吸收液。
①用离子方程式解释吸收液中含有
的原因:_____________;
②吸收液中的
、
均对NO2具有吸收作用,但
对NO2的吸收能力比
弱,
与NO2反应生成
的离子方程式是:___________;
(2)经测定,在烟气的吸收过程中,吸收液对NO2的吸收率随烟气通入量变化的曲线如下图所示。
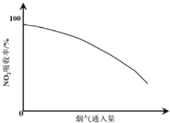
结合化学用语解释产生上述结果的原因:_______________。
高三化学填空题中等难度题查看答案及解析
-
与铀氮化物是重要的核燃料,已知某温度下三碳酸铀酰铵可发生如下分解反应:
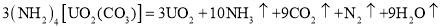 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为。
回答下列问题:
(1)
发生裂变反应:
,净产生的中子(
)数为________。基态
原子的外围电子排布式为
,则处于下列状态的铀原子或离子失去一个电子所需的能量最高的为________(填序号)。
A
B
C
D
(2)
和
中,沸点较高的为________,与
形成的配离子稳定性较高的为________。
(3)
中存在大
键,形成该大
键的电子数为________。
(4)某种铀氮化物的晶体结构与
相同。
的Bom-Haber循环如图所示。
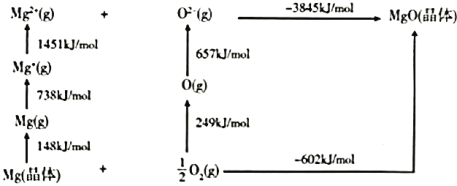
①
晶格能为________
。
②
的第二电离能大于
的第二电离能,是由于
的半径较
小、
的核电荷更高以及_______。
(5)另一种铀氮化物的晶胞如下图所示,
“原子”作面心立方最密堆积。
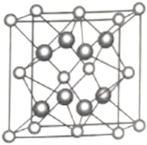
①铀元素的化合价为________,
“原子”的配位数为________。
②已知晶胞参数为
,则晶体的密度为________
(列出计算式)。
高三化学填空题困难题查看答案及解析
-
一种长效、缓释阿司匹林的合成路线如下图所示:
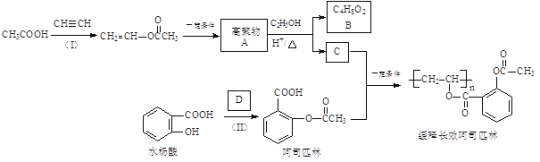
完成下列填空:
已知: RCOOR′+R"OH
RCOOR"+R′OH(R、R′、R"代表烃基)
(1)结构简式:A______________,B_______________;
(2)反应(Ⅰ)的反应类型为_________________,缓释长效阿司匹林结构中与“缓释作用”有关的官能团的名称为________________。
(3)D为乙酸酐,结构简式为
,写出一种与D互为同分异构体且能发生银镜反应的酯类的结构简式:__________。
(4)已知水杨酸酸性主要来源于“
”,阿司匹林中将“
”转化为“
”能大大降低对肠胃的刺激,由此你可以得出的结论是_________。
(5)已知:①乙炔与无机酸的反应和反应(Ⅰ)类似;②
,现以乙炔、甲醇为原料,无机试剂任选,合成丙烯酸甲酯(
)_________。(合成路线常用的表示方式为:
)
高三化学填空题中等难度题查看答案及解析