25℃时,向20 mL 0.0100 mol/L苯酚( )溶液中滴加0.0100 mol/LNaOH溶液,溶液的pH 与所加NaOH溶液体积(V)的关系如图所示。下列说法正确的是
)溶液中滴加0.0100 mol/LNaOH溶液,溶液的pH 与所加NaOH溶液体积(V)的关系如图所示。下列说法正确的是

A.25℃时,苯酚的电离常数Ka约为1.0×10-4
B.M点时,所加人NaOH 溶液的体积大于10 mL
C.M点时,溶液中的水不发生电离
D.加入20 mLNaOH溶液时,溶液中c(OH-)-c(H+)=2c(Na+)-2c()-c(
)
高三化学单选题困难题
25℃时,向20 mL 0.0100 mol/L苯酚( )溶液中滴加0.0100 mol/LNaOH溶液,溶液的pH 与所加NaOH溶液体积(V)的关系如图所示。下列说法正确的是
)溶液中滴加0.0100 mol/LNaOH溶液,溶液的pH 与所加NaOH溶液体积(V)的关系如图所示。下列说法正确的是

A.25℃时,苯酚的电离常数Ka约为1.0×10-4
B.M点时,所加人NaOH 溶液的体积大于10 mL
C.M点时,溶液中的水不发生电离
D.加入20 mLNaOH溶液时,溶液中c(OH-)-c(H+)=2c(Na+)-2c()-c(
)
高三化学单选题困难题
25℃时,向20 mL 0.0100 mol/L苯酚溶液中滴加0.0100 mol/LNaOH溶液,溶液的pH与所加NaOH溶液体积(V)的关系如图所示。下列说法正确的是( )
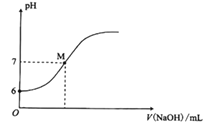
A.25℃时,苯酚的电离常数Ka约为1.0×10-12
B.M点时,所加入NaOH溶液的体积大于10 mL
C.加入20 mLNaOH溶液时,溶液中c(OH-)-c(H+)=c()
D.M点时,溶液中的水不发生电离
高三化学单选题中等难度题查看答案及解析
25℃时,向20 mL 0.0100 mol/L苯酚( )溶液中滴加0.0100 mol/LNaOH溶液,溶液的pH 与所加NaOH溶液体积(V)的关系如图所示。下列说法正确的是
)溶液中滴加0.0100 mol/LNaOH溶液,溶液的pH 与所加NaOH溶液体积(V)的关系如图所示。下列说法正确的是

A.25℃时,苯酚的电离常数Ka约为1.0×10-4
B.M点时,所加人NaOH 溶液的体积大于10 mL
C.M点时,溶液中的水不发生电离
D.加入20 mLNaOH溶液时,溶液中c(OH-)-c(H+)=2c(Na+)-2c()-c(
)
高三化学单选题困难题查看答案及解析
已知:苯酚(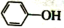 )在水中的电离方程式为
)在水中的电离方程式为 ,25℃时,苯酚的电离常数Ka=1.0×10-10。25℃时,用0.0100mol•L-1的NaOH溶液滴定20.00mL0.0100mol•L-1的苯酚溶液,溶液的pH与所加NaOH溶液的体积(V)的关系如图所示。下列说法正确的是
,25℃时,苯酚的电离常数Ka=1.0×10-10。25℃时,用0.0100mol•L-1的NaOH溶液滴定20.00mL0.0100mol•L-1的苯酚溶液,溶液的pH与所加NaOH溶液的体积(V)的关系如图所示。下列说法正确的是
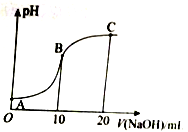
A. A点溶液中,苯酚的电离度约为0.01%
B. B点溶液的pH<7
C. C点溶液中存在c()>c(OH-)>c(H+)
D. A 点溶液加少量水稀释,溶液中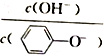 减小
减小
高三化学选择题困难题查看答案及解析
室温时,体积均为25.00mL,浓度均为0.0100mol•L-1的苯酚溶液、CH3COOH溶液及盐酸分别用0.0100mol•L-1NaOH溶液滴定,溶液的pH随V(NaOH)变化的曲线如图所示,下列说法正确的是( )
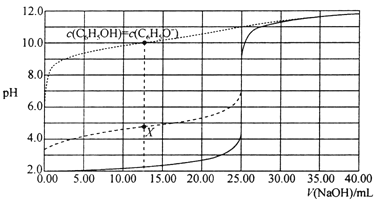
A.三个滴定过程中,均宜用甲基橙作指示剂
B.室温时,苯酚的电离平衡常数为1.0×10-10mol•L-1
C.X点对应的溶液中存在:c(CH3COO-)>c(CH3COOH)
D.物质的量浓度相同时,由水电离产生的c(OH-):C6H5ONa<CH3COONa<NaCl
高三化学多选题中等难度题查看答案及解析
下列图示与对应的叙述相符的是
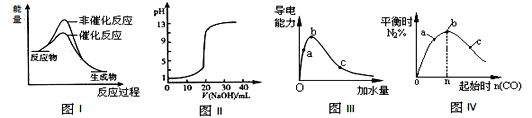
A.图I表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图Ⅱ表示常温下,0.1000mol/LNaOH溶液滴定20.00mL、0.0100mol/LHCl溶液所得到的滴定曲线
C.图Ⅲ表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c < a < b
D.图Ⅳ表示反应4CO(g)+2NO2(g) N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c > b > a
高三化学单选题困难题查看答案及解析
下列实验能获得成功的是
A.将乙醛滴入银氨溶液中制银镜
B.苯与浓溴水反应制取溴苯
C.在浓溴水中加几滴苯酚观察到白色沉淀
D.1mol/LCuSO4溶液5mL和 0.5mol/LNaOH溶液4mL混合后加入40%的乙醛溶液0.5mL,加热煮沸观察沉淀的颜色
高三化学选择题中等难度题查看答案及解析
下列图示与对应的叙述相符的是
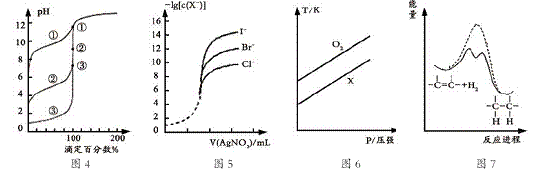
A. 用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由图4曲线确定①的酸性最强
B. 用0.0100mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,由图5曲线,可确定首先沉淀的是Cl-
C. 在体积相同的两个密闭容器中,分别充入相同质量O2和X气体,由图6可确定X可能是CH4气体
D. 由图7可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
高三化学选择题困难题查看答案及解析
下列图示与对应的叙述相符的是
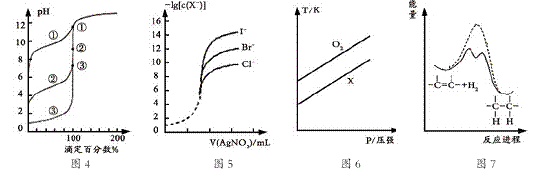
A. 用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由图4曲线确定①的酸性最强
B. 用0.0100mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,由图5曲线,可确定首先沉淀的是Cl-
C. 在体积相同的两个密闭容器中,分别充入相同质量O2和X气体,由图6可确定X可能是CH4气体
D. 由图7可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
高三化学选择题困难题查看答案及解析
常温下,用0.0100 mol/L的NaOH溶液滴定10. 00 mL 0.0100 mol/L的二元酸H2A,滴定过程中加入NaOH溶液的体积(V)与溶液中的关系如图所示,下列说法正确的是( )

A.H2A的电离方程式为:H2A=A2-+2H+
B.B点显酸性的原因是HA的电离程度大于其水解程度
C.C点溶液显中性,所以 c(Na+)=c(A2-) +c(HA-)
D.常温下Kh(Na2 A)的数量级约为10-4
高三化学单选题中等难度题查看答案及解析
25℃时,体积均为25. 00 mL,浓度均为0.0100 mol/L的HA、H3B溶液分别用0.0100mol/L NaOH溶液滴定,溶液的pH随V(NaOH)变化曲线如图所示,下列说法中正确的是
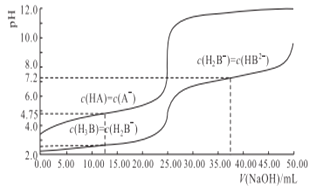
A.NaOH溶液滴定HA溶液可选甲基橙作指示剂
B.均为0. 0100 mol/L HA、H3B溶液中,酸性较强的是HA
C.25℃时,0. 0100 mol/L Na2HB溶液的pH >7
D.25℃时,向Na2HB溶液中滴加HA溶液反应的离子方程式为:HB2- + HA == H2B- + A-
高三化学多选题中等难度题查看答案及解析