-
(16分)间硝基苯胺(Mr=128)是一种重要的染料中间体。它是一种黄色针状结晶,微溶于水,随温度升高溶解度增大,溶于乙醇、乙醚、甲醇。间硝基苯胺可选用间二硝基苯与碱金属多硫化物进行选择性还原,其反应式如下:
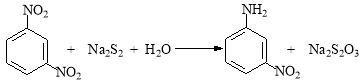
已知:R-NH2 + H+ → R-NH3+
实验步骤:
①在100mL锥形瓶中加入8g结晶硫化钠与30mL水,搅拌溶解。再加入2g硫黄粉,缓缓加热并不断搅拌到硫黄粉全部溶解,冷却后备用。
②在150mL三颈烧瓶中加入4.74g间二硝基苯(Mr=158)与40mL水,安装机械搅拌装置、滴液漏斗和回流冷凝管如图所示,将步骤①配制的多硫化钠溶液加入滴液漏斗。
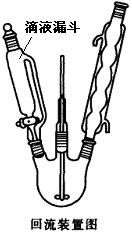
③加热三颈烧瓶至瓶内微微沸腾,开动搅拌使间二硝基苯与水形成悬浮液。慢慢滴加多硫化钠溶液,滴加完毕后继续搅拌回流30min。移去热源,用冷水浴使反应物迅速冷却到室温后,减压过滤,滤饼洗涤三次。
④在150mL某容器中配制稀盐酸(30mL水加7mL浓盐酸),将上述粗产物转移进该容器,加热并用玻璃棒搅拌,使间硝基苯胺溶解,冷却到室温后减压过滤。
⑤冷却滤液,在搅拌下滴加过量浓氨水到pH=8,滤液中逐渐析出黄色的间硝基苯胺。
⑥冷却到室温后减压过滤,洗涤滤饼到中性,抽干,产物重结晶提纯,在红外灯下干燥,称重,得2.56g。
回答下列问题:
(1)滴液漏斗较普通分液漏斗的优点 ;第④步中配制稀盐酸的容器名称为 。
(2)间二硝基苯和间硝基苯胺都有毒,因此该实验应在 内进行。
(3)在铁和盐酸作用制得初生态氢原子(还原性远强于碱金属多硫化物)也可以将硝基还原为氨基,却未被采用,其可能原因为 。
(4)第④步用盐酸溶解粗产品,而不用水的原因 。
(5)第③步中滤饼洗涤三次,可选用的洗涤剂为( );第⑥步产物要进行重结晶,可选用的试剂为( )。
A.冷水 B.热水 C.乙醚 D.乙醇
(6)第③步中,搅拌使间二硝基苯与水形成悬浮液后再滴加多硫化钠溶液,其原因为 。
(7)第⑥步中要将滤饼洗涤到中性,检验方法为 。
(8)该反应的产率为 。
-
对甲基苯胺可用对硝基甲苯在酸性条件下用铁粉还原制得:
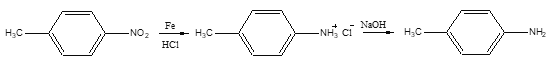
主要反应物和产物的物理性质见下表:
| 化合物 | 物质状态 | 溶解性 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) |
| 对硝基甲苯 | 浅黄色晶体 | 不溶于水,溶于乙醇、苯 | 51.4 | 237.7 | 1.286 |
| 对甲基苯胺 | 白色片状晶体 | 微溶于水,易溶于乙醇、苯 | 43~45 | 200~202 | 1.046 |
| 对甲基苯胺盐酸盐 | 白色晶体 | 易溶于水,不溶于乙醇、苯 | 243~245 | —— | —— |
| 苯 | 无色液体 | 不溶于水,溶于乙醇 | 5.5 | 80.1 | 0.874 |
实验流程如下:
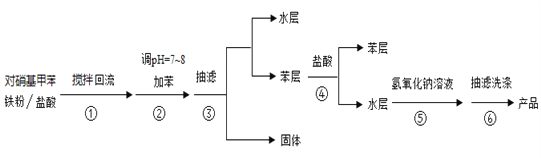
请回答下列问题:
(1)反应装置如图,a处缺少一装置_____________(填仪器名称)
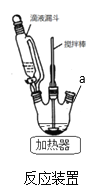
(2)步骤②中加苯的作用是_____________,步骤②中用5%碳酸钠溶液调pH=7~8的原因_________
(3)步骤③得到的固体物质为_________
(4)步骤④中加入盐酸的作用是_____________
(5)步骤⑤中通过加入氢氧化钠溶液使对甲基苯胺结晶析出的原理为_____________
(6)步骤⑥中,以下洗涤剂最合适的是_____________
A. 蒸馏水 B.乙醇 C.NaOH溶液 D.HCl溶液
-
乙酰苯胺是用途广泛的化工原料,主要应用于医药、日用化工等诸多领域。某兴趣小组制备流程如下:
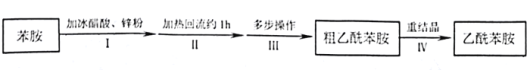
已知:
a.乙酰苯胺在水中的溶解度随温度的升高而增大
b.苯胺在空气中受热易被氧化
c.
| 名称 | 苯胺 | 醋酸 | 乙酰苯胺 |
| 沸点 | 184.4 | 117.9 | 304 |
d.反应原理: +CH3COOH
+CH3COOH 
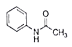 +H2O
+H2O
请回答:
(1)步骤Ⅰ,加入锌粉的目的__________。
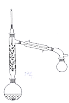
(2)步骤Ⅱ实验装置如图(加热装置省略),具体实验过程:装上一刺形分馏柱,插上温度计。用酒精灯加热,使反应溶液在微沸状态下回流,调节加热温度,使柱顶温度105℃左右,反应约 。在反应瓶上装一个刺形分馏柱,其作用是__________。
。在反应瓶上装一个刺形分馏柱,其作用是__________。
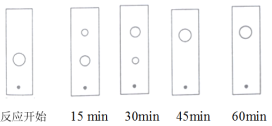
(3)步骤Ⅱ某同学采用薄层色谱(原理和操作与纸层析类同)跟踪反应进程,分别在反应开始、回流 、
、 、
、 和
和 时,用毛细管取样、点样、薄层色谱展开后的斑点如图所示。该实验条件下比较合适的回流时间是______。
时,用毛细管取样、点样、薄层色谱展开后的斑点如图所示。该实验条件下比较合适的回流时间是______。
A. B.
B. C.
C. D.
D.
(4)步骤Ⅳ,关于重结晶的操作,下列说法正确的是________。
A.选蒸馏水作为重结晶提纯乙酰苯胺的溶剂
B.粗制的有机化合物中常常含有有色杂质,可用活性炭进行脱色
C.趁热过滤时,需将菊花形滤纸放入长颈玻璃漏斗,一并放入保温漏斗中
D.趁热过滤也可以用减压过滤代替,提前将布氏漏斗放在沸腾的水浴中加热,防止乙酰苯胺热溶液遇到冷的布氏漏斗而提前析出。
E.冷却结晶时一般是在室温下自然冷却。当溶液降至室温,析出大量乙酰苯胺晶体后,可用冰水进一步冷却,以便晶体析出更加彻底。
(5)物质制备时,通常对纯度有一定要求,从结构与性质角度分析,上述制备过程中“由非氧化还原反应”产生的杂质可能有__________、_________。
-
己二酸是一种重要的化工原料和合成中间体。已知:室温下,己二酸微溶于水,当温度由28℃升至78℃时,其溶解度可增大20倍。某实验小组利用绿色氧化剂H2O2氧化环己烯合成己二酸,反应和制备装置如下:

主要实验步骤:
①在100mL三颈烧瓶中依次加入1.50g钨酸钠0.57g草酸和34mL30%过氧化氢溶液,室温下磁力搅拌20min。
②用恒压滴液漏斗缓慢加入8.0mL的环己烯,继续搅拌并加热回流2 小时,停 止加热。
③将反应液迅速转入烧杯中,冷却至室温后再用冰水浴冷却,有大量晶体析出。抽滤,并用少量冰水洗涤,即可得到己二酸晶体粗品。
回答下列问题:
(1)本实验中使用带刻度的恒压滴液漏斗的主要作用有_________、_________。
(2)步骤③中用冰水洗涤晶体的目的是______________________________________。
己二酸晶体粗品可利用_________方法进一步获得纯品。
(3)取0.1480g 己二酸(Mr=146.0)样品置于250mL锥形瓶中,加入50mL蒸馏水溶解,再加入2滴指示剂,用0.1000mol/Ld的NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为20.00 mL。
①本实验应选择_________(填“甲基橙”“石蕊”或“酚酞”)溶液作指示剂。
②判断滴定终点的方法是_________________________。
③样品中己二酸的质量分数为_________%(保留4位有效数字)。
(4)实验小组通过改变环己烯的用量来探究物料比对产率的影响,实验结果如下图所示。
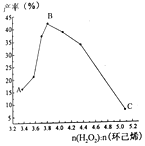
结合图像分析产率变化的可能原因:
①A点→B点:___________________________________________;
②B点→C点:____________________________________________。
-
(15 分) 亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
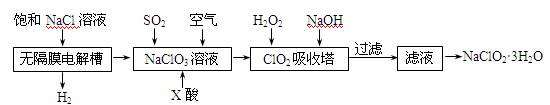
已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体只能保持在稀释状态下以防止爆炸性分解,且需现合成现用。
③ClO2气体在中性和碱性溶液中不能稳定存在。
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应方程式:________。
(2)反应生成ClO2气体需要X酸酸化的原因为:________。X酸为________。
(3)吸收塔内的温度不能过高的原因为:________
(4)吸收塔内ClO2随着还原剂的不同和溶液酸碱性的变化可被还原为ClO2—或Cl—。ClO2被S2—还原为ClO2—、Cl—的转化率与溶液pH的关系如右图所示。

请写出pH≤2时ClO2与S2—反应的离子方程式:________。
(5)第二步向NaClO3溶液中通SO2的同时通入空气的原因为:________。
(6)从滤液中得到NaClO2·3H2O粗晶体的操作步骤为
________、________、________。
-
(1 3分)亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:

已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体在中性和碱性溶液中不能稳定存在。
回答下列问题:
(1)在无隔膜电解槽中用惰性电极电解一段时间,阳极电极反应方式为 ;生成ClO2气体的反应中所加X酸为 。
(2)吸收塔内的温度不宜过高的原因为 ;ClO2吸收塔内发生反应的离子方程式为 。
(3)从溶液中得到NaClO2·3H2O粗晶体的实验操作名称依次是 ;粗晶体进一步提纯的实验操作名称是 。
(4)a kg 30% H2O2 理论上可最多制得 kg NaClO2 ·3H 2O
-
在自来水消毒和工业上砂糖、油脂的漂白与杀菌过程中,亚氯酸钠(NaClO2)发挥着重要的作用。下图是生产亚氯酸钠的工艺流程图:
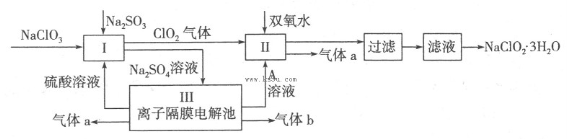
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O;
②常温下,Ksp(FeS)=6.3×10-18;Ksp(CuS)=6.3×10-28;Ksp(PbS)=2.4 ×10-28
(1)反应I中发生反应的离子方程式为 。
(2)从滤液中得到NaClO2·3H2O晶体的所需操作依次是 (填写序号)。
a.蒸馏 b.蒸发浓缩 c.过滤 d.冷却结晶 e.灼烧
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2。下表是25℃时HClO2及几种常见弱酸的电离平衡常数:
| 弱酸 | HClO2 | HF | H2CO3 | H2S |
| Ka/mol·L-1 | 1×10-2 | 6.3×10-4 | K1=4.30×10-7 K2=5.60×10-11 | K1=9.1×10-8 K2=l.1×10-12 |
①常温下,物质的量浓度相等的NaClO2、NaF、NaHCO3、Na2S四种溶液的pH由大到小的顺序为 (用化学式表示);体积相等,物质的量浓度相同的NaF、NaClO2两溶液中所含阴阳离子总数的大小关系为: (填“前者大”“相等”或“后者大”)。
②Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是 ;常温下,当最后一种离子沉淀完全时(该离子浓度为10-5mol·L-1)此时体系中的S2-的浓度为 。
(4)Ⅲ装置中生成气体a的电极反应式 ,若生成气体a的体积为1.12L(标准状况),则转移电子的物质的量为 。
-
在自来水消毒和工业上砂糖、油脂的漂白与杀菌过程中,亚氯酸钠(NaClO2)发挥着重要的作用。下图是生产亚氯酸钠的工艺流程图:

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出
NaClO2·3H2O;
②常温下,Ksp(FeS)=6.3×10-18;Ksp(CuS)=6.3×10-28;Ksp(PbS)=2.4 ×10-28
(1)反应I中发生反应的离子方程式为________________________________________________ 。
(2)从滤液中得到NaClO2·3H2O晶体的所需操作依次是________________________________________________ (填写序号)。
a.蒸馏 b.蒸发浓缩 c.过滤 d.冷却结晶 e.灼烧
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2。下表是25℃时HClO2及几种常见弱酸的电离平衡常数:
| 弱酸 | HClO2 | HF | H2CO3 | H2S |
| Ka/mol·L-1 | 1×10-2 | 6.3×10-4 | K1=4.30×10-7 K2=5.60×10-11 | K1=9.1×10-8 K2=l.1×10-12 |
①常温下,物质的量浓度相等的NaClO2、NaF、NaHCO3、Na2S四种溶液的pH由大到小的顺序为________________________________________________________ (用化学式表示);体积相等,物质的量浓度相同的NaF、NaClO2两溶液中所含阴阳离子总数的大小关系为:________________________________________________________________________________________________________________ (填“前者大”“相等”或“后者大”)。
②Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是 ________________________________________________________;常温下,当最后一种离子沉淀完全时(该离子浓度为10-5mol·L-1)此时体系中的S2-的浓度为 ________________________________________________________________________ 。
(4)Ⅲ装置中生成气体a的电极反应式 ________________________________________________________________________,若生成气体a的体积为1.12L(标准状况),则转移电子的物质的量为________________________ 。
-
亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
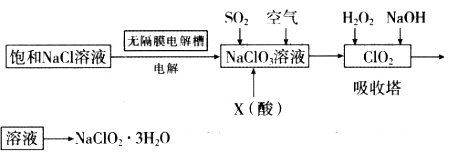
已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体在中性和碱性溶液中不能稳定存在。
回答下列问题:
(1)用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的_________(填化学式),至沉淀不再产生后。再加入过里的Na2CO3和NaOH,充分反应后将沉淀一并滤去。在无隔膜电解槽中用惰性电极电解一段时间生成NaClO3,阳极反应式为_______
(2)X酸是_________。写出二氧化氯发生器中生成ClO2的化学方程式_______,吸收塔内的温度不宜过高的原因为________
(3)亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2有毒,经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列分析正确的是(_____)
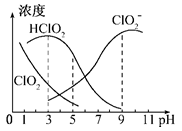
A.亚氯酸钠在碱性条件下较稳定
B.25℃时,HClO2的浓度随PH增大而增大
C.PH=6时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 25℃时,该溶液在pH=4时比pH=2时更适合漂白
(4)aKg 30%的双氧水理论上可最多制得___Kg NaClO2·3H2O
-
亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
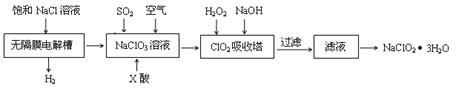
已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体只能保持在稀释状态下以防止爆炸性分解,且需现合成现用。
③ClO2气体在中性和碱性溶液中不能稳定存在。
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应方程式:________。
(2)反应生成ClO2气体需要X酸酸化的原因为:________。X酸为________。
(3)吸收塔内的温度不能过高的原因为:________
(4)吸收塔内ClO2随着还原剂的不同和溶液酸碱性的变化可被还原为ClO2—或Cl—。ClO2被S2—还原为ClO2—、Cl—的转化率与溶液pH的关系如右图所示。
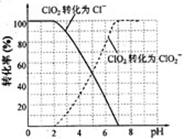
请写出pH≤2时ClO2与S2—反应的离子方程式:________。
(5)第二步向NaClO3溶液中通SO2的同时通入空气的原因为:________。
(6)从滤液中得到NaClO2●3H2O粗晶体的操作步骤为
________、________、________。






 +H2O
+H2O











