-
化学反应原理揭示了不同的物质在水溶液中有不同的行为。请按要求回答下列问题:(已知:H2SO3: Ka1=1.7×10-2,Ka2=6.0×10-8 ; NH3·H2O:Kb=1.8×10-5)
(1)将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈_________性,该溶液中各离子浓度由大到小的顺序为:_____________________________________________,所得溶液中c(H+)- c(OH-)=___________________________(填写表达式)
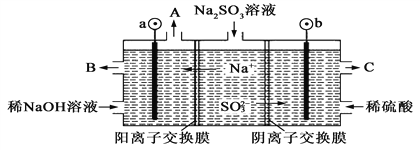
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如右图所示(电极材料为石墨)。
① 图中a极要连接电源的(填“正”或“负”)________极;C口流出的物质是________。
②SO32-放电的电极反应式为______________________________。
-
化学反应原理揭示了不同的物质在水溶液中有不同的行为。请按要求回答下列问题:(已知:H2SO3: Ka1=1.7×10-2,Ka2=6.0×10-8 ; NH3·H2O:Kb=1.8×10-5)
(1)将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈_________性,该溶液中各离子浓度由大到小的顺序为:_______________,所得溶液中c(H+)-c(OH-)=_______________(填写表达式)
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。

①图中a极要连接电源的(填“正”或“负”)________极;C口流出的物质是________。
② 放电的电极反应式为_______________。
放电的电极反应式为_______________。
-
物质在水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值(25℃):
HClO:Ka=3×10-8,HCN:Ka=4.9×10-10
H2CO3:Ka1=4.3×10-7,Ka2=5.6×10-11
(1)84消毒液中通入少量的CO2,该反应的化学方程式为______.
(2)25℃时,等物质的量浓度的①NaClO溶液;②Na2CO3溶液;③NaCN溶液,三溶液的pH由大到小的顺序为______(填序号).
(3)等物质的量NaClO和NaHCO3的混合液中,各微粒浓度的关系为:[Na+]=______+[H2CO3]
(4)实验室可用如图所示装置制备84消毒液,则a为______极,制备过程中总的离子反应方程式为______ ClO-+H2↑

-
雾霾天气严重影响人们的生活和健康。因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染。请回答下列问题:
(1)已知H2SO3的Ka1=1.3×10−2,Ka2=6.2×10−8,常温下,氢氧化钠溶液吸收SO2,若恰好生成NaHSO3,则溶液中c(SO32-)____c(H2SO3)(填 >、< 或 =)。
(2)已知汽车汽缸中NO的生成反应为:N2(g)+ O2(g) 2NO(g)△H>0。恒温、恒压密闭容器中,下列说法能说明该反应达到化学平衡状态的是_____。
2NO(g)△H>0。恒温、恒压密闭容器中,下列说法能说明该反应达到化学平衡状态的是_____。
a.氮气、一氧化氮消耗速率相等 b.N2、O2、NO的物质的量之比为1:1:2
c.氧气的转化率不再变化 d.混合气体的密度不再变化
(3)汽车使用乙醇汽油并不能减少NOx的排放。某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。
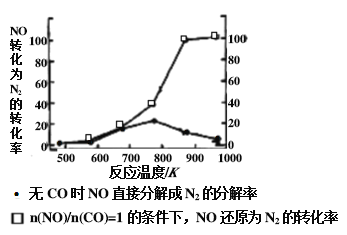
①若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为____。
②在n(NO)/n(CO)=1的条件下,为更好的除去NO物质,应控制的最佳温度在_____K左右。
(4)活性炭可处理大气污染物NO。在5 L密闭容器中加入NO和活性炭(无杂质),一定条件下反应生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
| 温度℃ 物质 | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
①写出NO与活性炭反应的化学方程式___________
②根据上述信息判断,T1和T2的关系是_______(填序号)。
a.T1>T2 b.T1<T2 c.无法比较
(5)Li—SO2电池具有输出功率高且低温性能好等特点,其电解质为LiBr,溶剂是碳酸丙烯酯和乙腈,Li+可在其中移动。电池总反应式为2Li+2SO2 Li2S2O4,则充电时阳极的电极反应式____。
Li2S2O4,则充电时阳极的电极反应式____。
-
25℃时,将SO2通入蒸馏水中模拟酸雨形成过程,实验数据如图。已知Ka1(H2SO3)=10-2,Ka2(H2SO3)=10-7。下列说法不正确的是
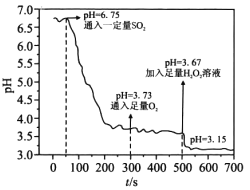
A. 300s未通O2时溶液中c(H2SO3)=10 -5.46mol·L-1
B. 400s时溶液中c(HSO3-)+c(SO32-)+c(SO42-)+c(H2SO3)≈10-3.73mol·L-1
C. 600s时,溶液中c(H+)约为c(SO42-)2倍
D. 由图推知,H2O2氧化性大于O2
-
物质在水溶液中有不同的行为。按要求回答下列问题:
(1)Na2SO3溶液显碱性,其原因是______________________________(用离子方程式表示),该溶液中各离子浓度由大到小的顺序为______________________。
(2)室温下向10mL氨水溶液中加水稀释后,下列量增大的有__________(填编号,下同),减小的有___________,不变的有____________。
a.溶液中离子浓度 b.氨水的电离程度
c.水的离子积常数 d.c(H+)/ c(NH3·H2O)
(3)亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。NaClO2变质可分解为NaClO3和NaCl。取等质量已变质和未变质的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量 (填“相同”或“不相同”),其原因是 。
-
已知H2SO3⇌HSO3-+H+,Ka1;HSO3-⇌SO32-+H+,Ka2。常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-、SO32-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )

A.pH=1.2溶液中:c(Na+)+c(H+)=c(OH-)+c(H2SO3)
B.常温下, =1000
=1000
C.向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离度先增大后减小
D.曲线3表示的微粒是SO32-
-
弱电解质在水溶液中存在多种平衡,它们在工农业生产中都有广泛的应用。已知如表数据,请回答下列问题:
| 化学式 | 温度(℃) | 平衡常数 |
| HClO | 25 | K=3.0×10-8 |
| H2CO3 | 25 | Ka1=4.5×10-7 Ka2=4.7×10-11 |
| H2O | 25 | Kw=10-14 |
(1)向NaClO溶液中通入少量CO2,所发生的离子方程式为________;
(2)等pH的NaClO、NaHCO3与Na2CO3溶液,则物质的量浓度最大的是________;
(3)向0.1mol/L的HClO溶液中滴加NaOH溶液至3c(HClO)=c(ClO-),此时混合溶液的pH=____;
(4)已知:NaA+CO2(少量)+H2O=HA+NaHCO3,NaB+CO2(少量)+H2O=HB+Na2CO3,则HA酸性___HB的酸性(填“强于”“弱于”“无法确定”)。
-
磷酸是重要的化学试剂和工业原料。请回答下列问题:
(1) 已知:25℃时,磷酸和氢氟酸的电离常数如下表所示。
| 物质 | H3PO4 | HF |
| 电离常数 | Ka1=7.1×10-3,Ka2=6.3×10-8, Ka1=4.2×10-13 | Ka=6.6×10-4 |
向 NaF 溶液中滴加少量 H3PO4溶液,反应的离子方程式为_____________。
(2) 已知:
Ⅰ.CaO(s)+H2SO4(l)  CaSO4(s)+H2O(l) ΔH=-271 kJ·mol-1
CaSO4(s)+H2O(l) ΔH=-271 kJ·mol-1
Ⅱ.5CaO(s)+3H3PO4(l)+HF(g)  Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ·mol-1
Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ·mol-1
则:①工业上用Ca5(PO4)3F和硫酸反应制备磷酸的热化学方程式为_____________。
②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率_______(填“ 增大”“ 减小”或“ 不变”,下同); HF的平衡浓度__________。
(3)工业上用磷尾矿制备Ca5(PO4)3F时生成的副产物 CO 可用于制备 H2,原理为
CO(g)+H2O(g)  CO2(g)+H2(g) ΔH。
CO2(g)+H2(g) ΔH。
①一定温度下,向 10 L 密闭容器中充入0.5 mol CO和 1 mol H2O(g),2 min 达到平衡时,测得 0~2 min 内用 CO2 表示的反应速率 v(CO2)=0.02 mol·L-1·min-1。则 CO的平衡转化率 α=________;该反应的平衡常数 K=______________。
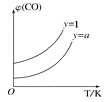
②在压强不变的密闭容器中发生上述反应,设起始的 ,CO 的平衡体积分数(φ)与温度(T) 的关系如图所示。
,CO 的平衡体积分数(φ)与温度(T) 的关系如图所示。
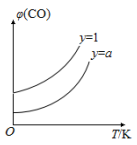
则:该反应的 ΔH________0(填“>” “ <” 或“=”,下同)。 a______1,理由为_______________。
-
磷酸是重要的化学试剂和工业原料。请回答下列问题:
(1)已知:25℃时,磷酸和氢氟酸的电离常数如下表所示。
| 物质 | H3PO4 | HF |
| 电离常数 | Ka1=7.1×10-3;Ka2=6.3×10-8;Ka3=4.2×10-13 | Ka=6.6×10-4 |
向NaF溶液中滴加少量H3PO4溶液,反应的离子方程式为___。
(2)已知:Ⅰ.CaO(s)+H2SO4(l)⇌CaSO4(s)+H2O(l) ΔH=-271kJ•mol-1
Ⅱ.5CaO(s)+3H3PO4(l)+HF(g)⇌Ca5(PO4)3F(s)+5H2O(l) ΔH=-937kJ•mol-1
则:①工业上用Ca5(PO4)3F和硫酸反应制备磷酸的热化学方程式为___。
②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率___(填“增大”“减小”或“不变”,下同);HF的平衡浓度___。
(3)工业上用磷尾矿制备Ca5(PO4)3F时生成的副产物CO可用于制备H2,原理为CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH。
①一定温度下,向10L密闭容器中充入0.5molCO和1molH2O(g),2min达到平衡时,测得0~2min内用CO2表示的反应速率v(CO2)=0.02mol•L-1•min-1。则CO的平衡转化率α=___;该反应的平衡常数K=___。
②在压强不变的密闭容器中发生上述反应,设起始的( )=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH___0(填“>”“<”或“=”,下同)。a___1,理由为___。
)=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH___0(填“>”“<”或“=”,下同)。a___1,理由为___。

放电的电极反应式为_______________。






