-
X、Y、Z、W为短周期元素,且原子序数依次增大,X2-和Y+核外电子排布相同,X、Z位于同一主族,Z、W位于同一周期,W的最外层电子数是X、Y最外层电子数之和。下列说法不正确的是
A. 原子半径Y>Z>X
B. X 分别与Y、Z形成的化合物均至少有两种
C. 最高价氧化物对应水化物的酸性:W>Z
D. 氢元素在与X、Y、Z分别形成的化合物中,化合价均为+1
-
X、Y、Z、Q、R五种元素的原子序数依次增大.其中:X的最外层电子排布为 ;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
请回答下列问题:
 元素基态原子的电子排布式为 ______ ,它的最高价氧化物的水化物的化学式为 ______ 。
元素基态原子的电子排布式为 ______ ,它的最高价氧化物的水化物的化学式为 ______ 。
 分子的立体构型是 ______ ,中心原子的杂化方式是 ______ 。
分子的立体构型是 ______ ,中心原子的杂化方式是 ______ 。
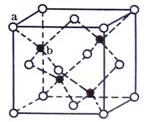
 与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为 ______。该晶体中与氮原子距离相等且最近的氮原子有 ______ 个。
与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为 ______。该晶体中与氮原子距离相等且最近的氮原子有 ______ 个。
 化合物
化合物 熔点为
熔点为 ,沸点为
,沸点为 ,熔融态不导电,可知
,熔融态不导电,可知 的晶体类型是 ______
的晶体类型是 ______  与热水反应的化学方程式为 ______ 。
与热水反应的化学方程式为 ______ 。
-
(12分)已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B;C、D与E分别位于同一周期。A原子L层上有2对成对电子, B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,,CE、FA为电子数相同的离子晶体。
(1)写出A元素的基态原子价电子排布式 ;F离子电子排布式 。
(2)写出X的化学式 和化学名称 。
(3)写出X涉及化工生产中的一个化学方程式 。
(4)试解释工业冶炼D不以DE3而是以D2A3为原料的原因: 。
(5)CE、FA的晶格能分别为786 KJ/mol l、3401KJ/mo,试分析导致两者晶格能差异的主要原因是: 。
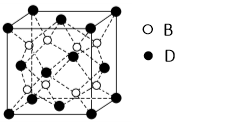
(6)F与B可形成离子化合物,其晶胞结构如图所示: F与B形成离子化合物的化学式为____________;该离子化合物晶体的密度为a g/cm3,则晶胞的体积是(只要求列出算式)。
-
已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A、B与C;D、E与F分别位于同一周期。A原子L层上有3个未成对电子,B的简单负二价离子与C原子核外电子排布相同、含有D元素的盐的焰色反应火焰为黄色,EF3是由活泼金属和活泼非金属组成的共价化合物,G有多种氧化物,其中一种氧化物有磁性,填写下列空白
(1)元素的第一电离能最大的是________, 属于过渡元素的是________(填写元素符号)
(2)写出B元素的基态原子价电子排布式__________________,F离子电子排布式_________________。
(3)AF3分子中A原子的杂化类型是________,AF3分子的几何构型为___________。
(4)已知E2B3的晶格比DF的晶格能大得多,试分析导致两者晶格能差异的主要原因是:________________________________________________________。
(5)构成G晶体的微粒是________,G的晶胞结构如下图甲所示,G的晶胞为________结构。若G原子的半径为1.27×10-10 m,G金属晶体中的晶胞长度,即下图乙中AB的长度为________m。

-
位于元素周期表前四周期的五种元素A、B、C、D、E,原子序数依次增大.A元素原子的最外层电子排布可表示为:asaap2a,B元素在地壳中含量居第二位,C与B位于同一周期,且是该周期元素中电负性最大的元素,D元素的+3价离子的3d亚层为半充满,E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.
根据以上信息回答下列问题:
(1)E的元素符号为______,其基态原子的电子排布式为______.
(2)A的氢化物比下周期同族元素的氢化物沸点还要高,其原因是______.
(3)B元素可分别与A元素、C元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为______(用化学式表示),原因是______.
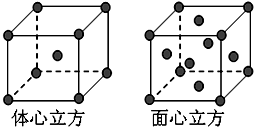
(4)D元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如下图所示.面心立方晶胞和体心立方晶胞中实际含有的D原子个数之比为______,两种堆积模型中与该元素一个原子等距离且最近的原子数之比为:______.
-
已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B;C、D与E分别位于同一周期。A原子L层上有2对成对电子, B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体,CE、FA为电子数相同的离子晶体。
(1)写出A元素的基态原子价电子排布式____________。
(2)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:___________。
(3)许多+l价铜的配合物溶液能吸收CO和烯烃(如C2H4等), CH3CH= CH 2 分子中3个C原子采取的杂化方式依次为___________。
(4)在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后沉淀完全溶解。写出此蓝色沉淀溶解的离子方程式:_____________;
(5)B的氢化物比氨气的熔沸点略高,请解释原因:_____________;
(6)1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家。C60分子是形如球状的多面体(如图),该结构的建立基于以下考虑:
①C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②C60分子只含有五边形和六边形;
③多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2。
据上所述,可推知C60分子有12个五边形和20个六边形。

请回答下列问题:
1)试估计C60跟F2在一定条件下,能否发生反应生成C60F60(填“可能”或“不可能”)__________,并简述其理由:_______________。
2)C70和C60结构类似,则分子中含有______个六边形和______个五边形。
-
【化学——选修3:物质结构与性质】
E、G、M、Q、T是五种原子序数依次增大的前四周期元素。E、G、M是位于P区的同一周期的元素,M的价层电子排布为nsnnp2n,E与M原子核外的未成对电子数相等;QM2与GM2-为等电子体;T为过渡元素,其原子核外没有未成对电子。请回答下列问题:
(1)与T同区、同周期元素原子价电子排布式是 。
(2)E、G、M均可与氢元素形成氢化物,它们的最简单氢化物在固态时都形成分子晶体,其中晶胞结构与干冰不一样的是 (填分子式)。
(3)E、G、M的最简单氢化物中,键角由大到小的顺序为 (用分子式表示),其中G的最简单氢化物的VSEPR模型名称为 ,M的最简单氢化物的分子立体构型名称为 。
(4)EM、GM+、G2互为等电子体,EM的结构式为(若有配位键,请用“→”表示) 。E、M电负性相差1.0,由此可以判断EM应该为极性较强的分子,但实际上EM分子的极性极弱,请解释其原因 。
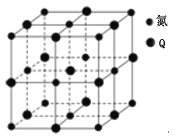
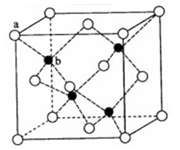
(5)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如下图所示,该晶体的密度为ρ g·cm-3。如果TQ的摩尔质量为M g/mol,阿伏加德罗常数为NA mol-1,则a、b之间的距离为 cm。
-
已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素。A与B,C、D与E分别位于同一周期。A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体。
(1)写出A元素的基态原子价电子排布式__________;F离子电子排布式为__________。
(2)写出X的化学式__________________________,化学名称为_________________。
(3)写出X涉及金属冶炼中的一个化学方程式_______________________________。
(4)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:
________________________________________________________________________。
(5)CE、FA的晶格能分别为786 kJ·mol-1、3 401 kJ·mol-1,试分析导致两者晶格能差异的主要原因是_______________________________________
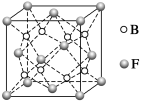
(6)F与B可形成离子化合物,其晶胞结构如图所示:F与B形成离子化合物的化学式为________;该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是________________(只要求列出算式)。
-
E、G、M、Q、T是五种原子序数依次增大的前四周期元素。E、G、M是位于P区的同一周期的元素,M的价层电子排布为nsnnp2n,E与M原子核外的未成对电子数相等;QM2与GM2-为等电子体;T为过渡元素,其原子核外没有未成对电子。请回答下列问题:
(1)与T同区、同周期元素原子价电子 排布式是 。
排布式是 。
(2)E、G、M均可与氢元素形成氢化物,它们的最简单氢化物在固态时都形成分子晶体,其中晶胞结构与干冰不一样的是 (填分子式)。
(3)E、G、M的最简单氢化物中,键角由大到小的顺序为 (用分子式表示),其中G的最简单氢化物的VSEPR模型名称为 ,M的最简单氢化物的分子立体构型名称为 。
(4)EM、GM+、G2互为等电子体,EM的结构式为(若有配位键,请用“→”表示) 。E、M电负性相差1.0,由此可以判断EM应该为极性较强的分子,但实际上EM分子的极性极弱,请解释其原因 。
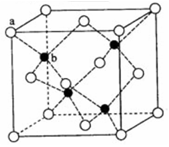
(5)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为ρ g·cm-3。如果TQ的摩尔质量为M g/mol,阿伏加德罗常数为NA mol-1,则a、b之间的距离为 cm。
-
E、G、M、Q、T是五种原子序数依次增大的前四周期元素。E、G、M是位于p区的同一周期的元素,M的价层电子排布为ns2np2n,E与M原子核外的未成对电子数相等;QM2与GM2-具有相等的价电子总数;T为过渡元素,其原子核外没有未成对电子。请回答下列问题:
(1)T元素原子的价电子排布式是__________。
(2)E、G、M三种元素的第一电离能由大到小的顺序为__ (用元素符号表示),其原因为________。
(3)E、G、M的最简单氢化物中,键角由大到小的顺序为 (用分子式表示),其中G的最简单氢化物的分子立体构型名称为_____ ___,M的最简单氢化物的分子中中心原子的杂化类型为 。M和Q的最简单氢化物的沸点大小顺序为__________(写化学式)。
(4)EM、GM+、G2互为等电子体,EM的结构式为(若有配位键,请用“→”表示)。E、M电负性相差1.0,由此可以判断EM应该为极性较强的分子,但实际上EM分子的极性极弱,请解释其原因: 。
(5) TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为pg·cm-3。如果TQ的摩尔质量为Mg.mol-1,阿伏加德罗常数为NA mol-1,则a、b之间的距离为_______cm。