-
(8分)用符号“>”“<”或“=”连接下列各项关系。
(1)第一电离能N______O; (2)电负性:N______C;
(3)键的极性:H-C______H-Si ; (4)键角:H2S______NH3
(5)分子中σ键数目:C6H6______C3H8; (6)分子中π键数目:C2H4______C2H2
(7)晶格能:MgO______KI (8)原子化热:Na ______K
高三化学填空题简单题查看答案及解析
-
用符号“>”或“<”表示下列各项关系。
(1)第一电离能:Na __________ Mg,Mg _______ Ca。
(2)电负性:O ________ F,F ________ Cl。
(3)能量高低:ns ________ (n+1)s,ns ________ np。
高三化学填空题简单题查看答案及解析
-
SiC纤维单向增强的TixAly基复合材料可作为高超音速飞行器表面的放热材料。回答下列问题:
(1)C元素所在周期中,第一电离能最大的元素是__(填元素符号),电负性最大的是__(填元素符号)。
(2)基态Ti原子的价电子排布式为__,能量最高的能级有__个空轨道。
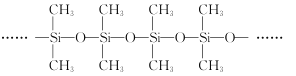
(3)甲基硅油结构如图所示,其中Si原子的杂化方式为__。以甲基硅油为主要成分的硅橡胶能够耐高温的原因是__。

(4)Li2CO3、Li2TiO3是锂离子电池中的常用材料,其中CO32-的空间构型为__,其含有的共价键类型有__。
(5)TixAly合金的一种结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),该合金的化学式为__。其结构单元棱长为apm,底面边长为bpm,该合金的密度为___g·cm-3。
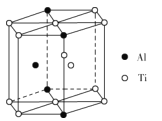
高三化学解答题中等难度题查看答案及解析
-
SiC纤维单向增强的TixAly基复合材料可作为高超音速飞行器表面的放热材料。回答下列问题:
(1)C元素所在周期中,第一电离能最大的元素是__(填元素符号),电负性最大的是__(填元素符号)。
(2)基态Ti原子的价电子排布式为__,能量最高的能级有__个空轨道。
(3)甲基硅油结构如图所示,其中Si原子的杂化方式为__。以甲基硅油为主要成分的硅橡胶能够耐高温的原因是__。
(4)Li2CO3、Li2TiO3是锂离子电池中的常用材料,其中CO32-的空间构型为__,其含有的共价键类型有__。
(5)TixAly合金的一种结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),该合金的化学式为__。其结构单元棱长为apm,底面边长为bpm,该合金的密度为___g·cm-3。
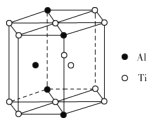
高三化学解答题中等难度题查看答案及解析
-
呋喃(
)和吡咯(
)是较常见的杂环化合物呋喃通过下列反应可转化为吡咯:
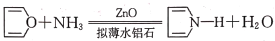
回答下列问题:
(1)呋喃和吡咯所含元素中:电负性最大的是___________(填元素符号),第一电离能最大的元素的基态原子电子排布图是______________________。
(2)呋喃分子中,碳原子的杂化方式是___________,1mol吡咯分子中含________molσ键。
(3)NH3与H2O可与Zn2+形成配合物[Zn(NH3)3(H2O)]2+。与Zn2+形成配位键的原子是___________(填元素符号);H2O的空间构型为___________;写出一种与NH3互为等电子体的阳离子:___________(填化学式)。
(4)NH3的相对分子质量比N2O的小,但其沸点却比N2O的高,其主要原因是___________。
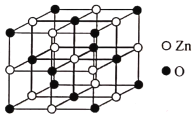
(5)ZnO晶体随着环境条件的改变能形成不同结构的晶体,其中一种的晶胞结构如图所示,已知该ZnO晶体密度为ag·cm-3,NA表示阿伏加德罗常数。则该晶体中与Zn2+等距离且最近的Zn2+共有___________个,该ZnO晶胞中相邻两个O2-之间的距离为___________nm。
高三化学综合题中等难度题查看答案及解析
-
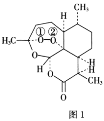
青蒿素是从黄花蒿中提取的一种无色针状晶体,其结构如图1,请回答下列问题:

(1)基态O原子的价电子排布图为___。
(2)组成青蒿素的三种元素中电负性最大的是__(填元素符号,下同),第一电离能最大的是__。
(3)基态N原子的未成对电子数为___。
(4)双氢青蒿素是青蒿素的重要衍生物,其抗疟疾疗效优于青蒿素,双氢青蒿素的合成一般是在相转移催化剂聚乙二醇的作用下,用硼氢化钠(NaBH4)还原青蒿素。两种硼氢化物的合成原理如下:
2LiH+B2H6=2LiBH4;4NaH+BF3=NaBH4+3NaF
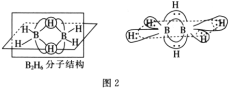
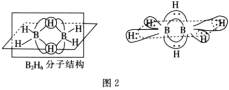
BH4-的空间构型为__;B2H6分子的结构如图2,B2H6中B的杂化方式为__。
聚乙二醇[HO(CH2CH2O)nH]随着n值的增大,水溶性降低,原因是___。
(5)NaH的晶胞与NaCl相同,NaH晶体中阳离子的配位数是__;设晶胞中阴、阳离子为刚性球体且恰好相切,阴、阳离子的半径比约为__(已知
≈1.414,结果保留三位有效数字)。
高三化学综合题中等难度题查看答案及解析
-
青蒿素是从黄花蒿中提取的一种无色针状晶体,其结构如图1,请回答下列问题:
(1)基态O原子的价电子排布图为___。
(2)组成青蒿素的三种元素中电负性最大的是__(填元素符号,下同),第一电离能最大的是__。
(3)基态N原子的未成对电子数为___。
(4)双氢青蒿素是青蒿素的重要衍生物,其抗疟疾疗效优于青蒿素,双氢青蒿素的合成一般是在相转移催化剂聚乙二醇的作用下,用硼氢化钠(NaBH4)还原青蒿素。两种硼氢化物的合成原理如下:
2LiH+B2H6=2LiBH4;4NaH+BF3=NaBH4+3NaF
BH4-的空间构型为__;B2H6分子的结构如图2,B2H6中B的杂化方式为__。
聚乙二醇[HO(CH2CH2O)nH]随着n值的增大,水溶性降低,原因是___。
(5)NaH的晶胞与NaCl相同,NaH晶体中阳离子的配位数是__;设晶胞中阴、阳离子为刚性球体且恰好相切,阴、阳离子的半径比约为__(已知
≈1.414,结果保留三位有效数字)。
高三化学综合题中等难度题查看答案及解析
-
H、N、O、S、Ni、As为元素周期表中1~4周期元素。请回答下列问题:
(1)上述元素中第一电离能最大的元素符号是___________,电负性最大的元素的原子其价电子轨道表示式为___________。
(2)CH3NO2中C和N的原子轨道杂化方式分别为___________、___________。
(3)SO32-其空间构型为___________。写出一种与该酸根等电子体的微粒___________。
(4)NH3极易溶于水其原因除二者都为极性分子外,另一个重要原因是___________。
(5)Ni与As形成的一种化合物,其晶体如图所示,属六方晶系。
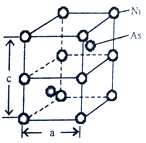
①该晶体的化学式为___________,As原子的配位数为___________。
②已知晶胞参数a=360.2pm,c=500.9pm,此晶体的密度为___________g·cm-3。(写出计算式,NA为阿伏加德罗常数的值)
高三化学综合题中等难度题查看答案及解析
-
已知X、Y、Z为第三周期元素,其原子的第一至第四电离能如下表:
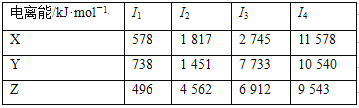
(1)则X、Y、Z的电负性从大到小的顺序为______________(用元素符号表示),元素Y的第一电离能大于X的第一电离能原因是___________________________________________。
(2)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小。D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C 三原子都采取sp3杂化。
①A、B、C的第一电离能由小到大的顺序为________________(用元素符号表示)。
②M是含有________键(填”极性”或”非极性”)的________分子(填”极性”或”非极性”)。
③N是一种易液化的气体,请简述其易液化的原因_________________________________。
④W分子的VSEPR模型的空间构型为________,W分子的空间构型为________。
⑤AB-离子中和B2分子的π键数目比为________。
(3)E、F、G三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1。
①E元素组成的单质的晶体堆积模型为________(填代号)。
a.简单立方堆积 b.体心立方堆积 c.六方最密堆积 d.面心立方最密堆积
②F元素在其化合物中最高化合价为________。
③G2+离子的核外电子排布式为___________________________________________,G2+和N分子形成的配离子的化学式为________。
高三化学填空题困难题查看答案及解析
-
(1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是(用元素符号表示)
(2)A、B、C为同一短周期金属元素。依据下表数据分析,C元素在化合物中的主要化合价为;第二电离能(I2)B小于A的原因是 。
电离能/kJ·mol-1
I1
I2
I3
I4
A
500
4600
6900
9500
B
740
1500
7700
10500
C
580
1800
2700
11600
(3)已知过氧化氢分子的空间结构如右图所示,分子中氧原子采取杂化;通常情况下,H2O2与水任意比互溶的主要原因是。
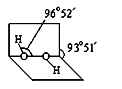
(4)R是1~36号元素中未成对电子数最多的原子。R3+在溶液中存在如下转化关系:
R3+
R(OH)3
[R(OH)4]-
①基态R原子的价电子排布式为________。
②[R(OH)4]-中存在的化学键是________。
A.离子键 B.极性键 C.非极性键 D.配位键
高三化学填空题中等难度题查看答案及解析